Storia

Una fotografia del 1893 di Jean-Martin Charcot, il quale ha dato importanti contributi nella comprensione della malattia e ne ha proposto il nome in onore di James Parkinson
Diverse fonti antiche, tra cui un papiro egiziano, un trattato di medicina Ayurveda, la Bibbia e gli scritti di Galeno, descrivono sintomi simili a quelli della malattia di Parkinson.[2] Dopo Galeno e fino alla fine del XVII secolo, non vi sono altri riferimenti chiari relativi alla malattia.[2] Nei secoli successivi, diversi autori hanno documentato le varie caratterisiche della malattia. Tra di essi ricordiamo: Franciscus Sylvius, Hieronymus David Gaubius, John Hunter e Auguste François Chomel.[2][3][4] Nel 1817 un medico inglese, James Parkinson, pubblicò un saggio in cui segnalava sei casi di paralisi agitante.[5] Parkinson descrisse il caratteristico tremore a riposo, la postura e l’andatura anomala, la paralisi, la diminuzione della forza muscolare e il modo in cui la condizione progredisce nel tempo.[5][6] I primi neurologi che hanno contribuito a comprendere meglio la malattia, comrendono: Armand Trousseau, William Richard Gowers, Samuel Alexander Kinnier Wilson, Wilhelm Heinrich Erb e più in particolare Jean-Martin Charcot, i cui studi effettuati tra il 1868 e il 1881 sono stati un punto di riferimento nella sua comprensione.[5] Tra le varie scoperte, Charcot, gli va attribuito il merito di aver compiuto la distinzione tra la rigidità, la debolezza e la bradicinesia.[5] Egli ha anche sostenuto la ridenominazione della malattia in onore di James Parkinson.[5] Nel 1912, Frederic Lewy descrisse le particelle microscopiche nel cervello colpito dalla malattia, poi chiamate “corpi di Lewy”.[5] Nel 1919, Konstantin Tretiakoff scoprì che la substantia nigra è la principale struttura cerebrale colpita, ma questa scoperta non fu ampiamente accettata fino a quando non è stata confermata da ulteriori studi pubblicati da Rolf Hassler nel 1938.[5] I cambiamenti biochimici alla base del cervello sono stati individuati nel 1950, grazie soprattutto al lavoro di Arvid Carlsson sul neurotrasmettitore dopamina e sull’identificazione del suo ruolo nella malattia.[7] Nel 1997, l’alfa-sinucleina è risultata essere il principale componente dei corpi di Lewy.[8] La somministrazione di anticolinergici e la chirurgia (lesione della via cortico-spinale o di alcune delle strutture dei gangli della base) sono stati i trattamenti utilizzati fino all’introduzione del farmaco levodopa, che ne ha ridotto drasticamente il loro uso.[3][9] La levodopa è stata sintetizzata nel 1911 da Kazimierz Funk, ma ricevette poca attenzione fino alla metà degli anni 20.[7] Entrò successivamente nella pratica clinica nel 1967, portando una rivoluzione nella gestione della malattia.[7][10] Alla fine del 1980 la stimolazione cerebrale profonda viene considerata essere un possibile trattamento.[11]
Epidemiologia
La malattia di Parkinson è la seconda malattia neurodegenerativa più comune dopo la malattia di Alzheimer.[12] La prevalenza della condizione nei paesi industrializzati è di circa lo 0,3%. La malattia di Parkinson è più comune negli anziani e la prevalenza aumenta dell’1% in quelli oltre i 60 anni di età e del 4% della popolazione sopra gli 80 anni.[12] L’età media di insorgenza è circa 60 anni, anche se il 5-10% dei casi, classificati come ad esordio giovane, iniziano tra i 20 e i 50 anni.[13] La malattia risulta essere meno diffusa nelle popolazioni di origine africana e asiatica, sebbene questo dato sia contestato.[12] Alcuni studi hanno proposto che sia più comune negli uomini rispetto alle donne, ma altri non hanno rilevato particolari differenze tra i due sessi.[12] L’incidenza della malattia di Parkinson è tra l’8 e il 18 per 100.000 persone-anno.[12]
Fattori di rischio

Un elicottero dell’US Army sparge l’Agente Arancio su terreni agricoli vietnamiti durante la guerra del Vietnam. L’Agente Arancio è stato correlato alla malattia di Parkinson.
Molti fattori di rischio e molti fattori protettivi sono stati proposti, a volte in relazione alle teorie riguardanti i possibili meccanismi della malattia, ma nessuno è stato definitivamente individuato da prove certe. Quando gli studi epidemiologici sono stati condotti per verificare la relazione tra un dato fattore e la malattia di Parkinson, spesso i risultati sono apparsi contraddittori.[12] Le correlazioni più frequentemente proposte per aumentarne il rischio, sono quelle in cui viene coinvolta l’esposizione ai pesticidi, mentre sembra esserci una riduzione del rischio nei fumatori.[12] Iniezioni della neurotossina MPTP sintetica producono una serie di sintomi simili a quelli della malattia di Parkinson, essi possono essere bloccati interrompendo l’assunzione di tale sostanza. L’osservazione di questo fenomeno ha portato a teorizzare che l’esposizione ad alcune tossine ambientali possa aumentare il rischio di sviluppare la condizione.[12] Le tossine che sono state correlate alla malattia e ritenute in grado di aumentare del doppio il rischio di soffrirne, comprendono alcuni pesticidi, quali il rotenone e il paraquat, e erbicidi, come l’Agente Arancio.[12][14][15] Le misure indirette dell’esposizione, come quelle effettuate su persone che vivono in ambienti rurali, hanno evidenziato un aumento del rischio di sviluppare la malattia di Parkinson.[15] Anche l’esposizione ai metalli pesanti è stata proposta come fattore di rischio per la malattia, attraverso il possibile accumulo nella substantia nigra, tuttavia gli studi sull’argomento si sono rivelati inconcludenti.[12] Alcuni studi hanno messo in correlazione il verificarsi di ripetuti traumi cranici e lo sviluppo della malattia.[16] Si sospetta che i pugili professionisti, a seguito dei violenti colpi al capo cui sono soggetti, possano sviluppare una sindrome di Parkinson di carattere progressivo (il caso di Cassius Clay ne potrebbe essere una dimostrazione).[16][17][18][19] Uno studio compiuto su praticanti boxe thailandese ritirati, ha evidenziato un aumento del rischio.[18] Da non trascurare, infine, l’ipotesi legata all’età. La malattia presenta un picco di insorgenza attorno ai sessant’anni, e nell’adulto sano la perdita di cellule e pigmento nella sostanza nera è maggiore proprio intorno al sessantesimo anno d’età. Viene meno così la protezione delle cellule contenenti dopamina e il cervello delle persone anziane è, inevitabilmente, più predisposto al Parkinson.[20][21] Si ritiene, inoltre, che disturbi psichiatrici, come la depressione, siano un ulteriore fattore di rischio per la malattia.[22] Secondo i dati elaborati da uno studio pubblicato nel 2011, tra le sostanze organiche che aumentano il rischio di sviluppare la patologia in caso di prolungata esposizione vi sono il tricloroetilene, il percloroetilene e il tetracloruro di carbonio[23].
Fattori di protezione

Struttura di una molecola di caffeina. È stato dimostrato che il suo consumo protegge dalla malattia di Parkinson.
È stato dimostrato che il consumo di caffeina è in grado di proteggere dalla malattia di Parkinson.[24] Studi epidemiologici condotti su ampie coorti (374.003 soggetti) hanno evidenziato che il rischio di sviluppare la condizione diminuisce progressivamente con il consumo di caffè e di altri alimenti contenenti caffeina.[25] Sebbene il fumo di tabacco sia devastante per la longevità e per la qualità della vita, è stato correlato ad una diminuzione del rischio di avere la malattia. Tale rischio, nei fumatori, può arrivare ad essere minore fino a un terzo rispetto ai non fumatori.[12] Il motivo di ciò non è noto con certezza, ma si ritiene che la nicotina possa avere un effetto stimolante sulla dopamina.[12][26] Il fumo di tabacco contiene composti che agiscono come inibitori della monoamino ossidasi che potrebbero anche loro contribuire a questo effetto.[27] Gli antiossidanti, come le vitamine C e D, sono stati proposti come sostanze protettive per proteggere contro la malattia, ma i risultati degli studi sono stati contraddittori e nessun effetto positivo è stato dimostrato.[12] Anche gli studi sull’assunzione di acidi grassi e grassi alimentari non hanno portato a risultati chiari.[12] Infine, vi sono state indicazioni preliminari di un possibile ruolo protettivo degli estrogeni e dei farmaci anti-infiammatori non steroidei.[12]
Patogenesi
Anatomia patologica

Un corpo di Lewy (colorato di marrone) in una cellula cerebrale della substantia nigra nella malattia di Parkinson. Il colore marrone è per via della colorazione immunoistochimica positiva alla alfa-sinucleina.
I gangli basali, un gruppo di “strutture cerebrali” innervate dal sistema dopaminergico, sono le aree cerebrali più colpite nella malattia di Parkinson.[28] La principale caratteristica patologica della condizione è la morte delle cellule nella substantia nigra e, più specificamente, nella parte ventrale (anteriore) della pars compacta, causando nel tempo la morte delle cellule fino al 70% del loro totale.[29] Al taglio del tronco cerebrale, si possono notare alterazioni macroscopiche in cui la perdita neuronale si può dedurre da una riduzione della pigmentazione della melanina nella substantia nigra e nel locus coeruleus.[30] L’istopatologia (anatomia microscopica) della substantia nigra e delle diverse regioni cerebrali, mostra una perdita neuronale e corpi di Lewy in molte delle cellule nervose rimanenti. La perdita neuronale è accompagnata da morte degli astrociti (cellule gliali a forma di stella) e l’attivazione delle microglia (un altro tipo di cellule gliali). I corpi di Lewy sono un elemento patologico chiave nella malattia di Parkinson.[30]
Fisiopatologia

L’immagine mostra le proiezioni dopaminergiche in una persona sana (a sinistra) e nella malattia di Parkinson (a destra). Le frecce rosse e blu rappresentano rispettivamente l’inibizione e la stimolazione della struttura di destinazione.

A. Schema della progressione iniziale dei depositi di corpi di Lewy nelle prime fasi del morbo di Parkinson, come proposto da Braak. B. Localizzazione della zona di significativa riduzione del volume cerebrale nel fase iniziale della malattia rispetto ad un gruppo di partecipanti sani ad uno studio di neuroimaging, che ha concluso che il danno al tronco cerebrale può essere la prima tappa identificabile della malattia di Parkinson.[31]
I sintomi principali della malattia di Parkinson sono il risultato di una attività molto ridotta delle cellule secernenti dopamina, causata dalla morte cellulare nella regione pars compacta della substantia nigra.[28] Nel cervello vi sono cinque circuiti principali che collegano le aree cerebrali ai gangli basali. Questi circuiti sono noti come: circuito motorio, circuito oculomotore, circuito associativo, circuito limbico e circuito orbitofrontale, con nomi che indicano la principali aree che vengono servite da ogni circuito.[28] Nella malattia di Parkinson, tutti i circuiti elencati possono venire influenzati e ciò spiega molti dei sintomi. Infatti, una varietà di funzioni sono controllate da questi circuiti, tra le quali quelle del movimento, dell’attenzione e dell’apprendimento.[28] Dal punto di vista scientifico, il circuito motorio è quello che è stato studiato con più attenzione.[28] Un particolare modello concettuale del circuito motorio e del suo coinvolgimento nella malattia è stato, a partire dal 1980, di grande influenza, anche se nel tempo sono stati sollevati alcuni dubbi che hanno portato a modificarlo.[28] In questo modello, i gangli della base normalmente esercitano un’influenza costante inibitoria su una vasta gamma di sistemi motrici, impedendo loro di attivarsi nei momenti inopportuni. Quando si decide di effettuare una determinata azione, l’inibizione viene ridotta. La dopamina agisce per facilitare questo cambiamento nell’inibizione: livelli elevati di dopamina tendono a promuovere l’attività motoria, mentre bassi livelli, come avviene nella malattia, richiedono maggiori sforzi per compiere un dato movimento. Così l’effetto reale della deplezione di dopamina è il verificarsi dell’ipocinesia, una riduzione complessiva dell’uscita dei segnali motori.[28] I farmaci che vengono usati per trattare la malattia di Parkinson, viceversa, tendono a produrre una quantità troppo elevata di dopamina, portando i sistemi motori ad attivarsi nel momento non appropriato e causando pertanto discinesia.[28]
Morte delle cellule cerebrali
Vi sono diversi meccanismi proposti per cui le cellule cerebrali, nella malattia, vanno incontro alla morte.[32] Uno di questi prevede che un accumulo anomalo della proteina alfa-sinucleina, legata alla ubiquitina, danneggi le cellule. Questa proteina insolubile si accumula all’interno dei neuroni forando delle inclusioni, chiamate corpi di Lewy.[29][8] Secondo la stadiazione di Braak, una classificazione della malattia sulla base del quadro patologico, i corpi di Lewy prima appaiono nel bulbo olfattivo, nel midollo allungato e nel tegmento pontino, con i pazienti che risultano asintomatici. Col progredire della malattia, i corpi di Lewy si sviluppano nella substantia nigra, nelle aree del mesencefalo e prosencefalo basale e, nell’ultima fase, nella neocorteccia.[29] Queste zone del cervello sono le aree principali della degenerazione neuronale nella malattia di Parkinson. Tuttavia, corpi di Lewy, non possono essere la causa diretta della morte delle cellule.[32][8] Nei pazienti con demenza una presenza generalizzata dei corpi di Lewy è comune nelle aree corticali. Ammassi neurofibrillari e placche senili, riscontrabili caratteristicamente nella malattia di Alzheimer, non sono comuni a meno che il paziente non presenti una forma di demenza.[30] Altri meccanismi che portano alla morte cellulare includono la disfunzione dei sistemi lisosomiali e proteosomiali e una ridotta attività mitocondriale.[32] L’accumulo di ferro nella substantia nigra si osserva tipicamente in combinazione con le inclusioni proteiche. Ciò può essere correlato allo stress ossidativo, all’aggregazione proteica e alla morte neuronale, ma i meccanismi che regolano questo fenomeno non sono pienamente compresi.[33]
Eziologia
La maggior parte delle persone con malattia di Parkinson presenta una condizione idiopatica (che non ha una causa specifica nota). Una piccola percentuale di casi, tuttavia, può essere attribuita a fattori genetici conosciuti. Altri fattori sono stati associati con il rischio di sviluppare la malattia, ma non sono stati dimostrate relazioni causali. La malattia di Parkinson è stata tradizionalmente considerata una malattia non genetica. Tuttavia, circa il 15% degli individui con malattia di Parkinson ha un parente di primo grado con la stessa condizione.[13] Almeno il 5% delle persone è ormai noto per avere forme della malattia che si verifica a causa di una mutazione di uno dei numerosi geni specifici.[34]

Struttura quaternaria della dardarina.
Le mutazioni in geni specifici sono state definitivamente dimostrate di essere causa della malattia. Questi geni codificano per alfa-sinucleina (SNCA), parkina (PRKN), dardarina (LRRK2), PTEN chinasi indotta putativo 1 (PINK1), DJ-1 e ATP13A2.[29][34] Nella maggior parte dei casi, le persone con queste mutazioni svilupperanno la malattia di Parkinson. Con l’eccezione di LRRK2, tuttavia, rappresentano solo una piccola minoranza dei casi della malattia.[29] I geni correlati alla condizione e più studiati geni sono SNCA e LRRK2. Le mutazioni nei geni tra cui SNCA, LRRK2 e glucocerebrosidasi (GBA) sono stati trovati per essere fattori di rischio per sviluppare malattia di Parkinson. Le mutazioni in GBA sono note per causare la malattia di Gaucher.[34] Il ruolo del gene SNCA è importante in quanto l’alfa-sinucleina alfa è il componente principale dei corpi di Lewy.[34] Mutazioni missenso del gene (in cui un singolo nucleotide viene cambiato) e duplicazioni e triplicazioni del locus che lo contiene, sono state trovate in diversi gruppi aventi familiari affetti dalla malattia di Parkinson.[34] Le mutazioni missenso sono rare.[34] Tuttavia, moltiplicazioni del locus SNCA rappresentano circa il 2% dei casi familiari.[34] Il gene LRRK2 (PARK8) codifica per una proteina chiamata dardarina. Il nome dardarina è stato coniato da una parola basca che sta per tremore, poiché questo gene è stato identificato in famiglie provenienti dall’Inghilterra e dal nord della Spagna.[29] Le mutazioni nel LRRK2 sono la causa più comune conosciuta di malattia di Parkinson famigliare e sporadica, esse rappresentano circa il 5 % degli individui con una storia familiare della malattia e il 3% dei casi sporadici.[29][34] Vi sono molte differenti mutazioni descritte in LRRK2, la prova inequivocabile di causalità esiste, tuttavia, solo per un piccolo numero.[34]
Segni e sintomi
La malattia di Parkinson colpisce prevalentemente il movimento, producendo sintomi motori.[35] Sintomi non motori, che comprendono insufficienza autonomica, problemi neuropsichiatrici (alterazioni dell’umore, della cognizione, del comportamento o del pensiero), difficoltà sensoriali e del sonno, sono anch’essi comuni.[35]
Movimento

Un uomo con il morbo di Parkinson, si noti la postura flessa (camptocormia). Foto apparsa in Nouvelle Iconographie de la Salpêtrière, vol. 5
Quattro caratteristiche motorie sono considerati come la base sintomatologica della malattia di Parkinson: il tremore, la rigidità, la bradicinesia e l’instabilità posturale.[35] Il tremore è il sintomo più evidente e più comune, anche se circa il 30% degli individui con malattia di Parkinson all’esordio non lo mostra.[35] Il tremore è tipicamente “a riposo”, con bassa frequenza, scompare durante i movimenti volontari e in genere peggiora nelle situazioni di stress emozionale, mentre è assente durante il sonno.[35] Esso coinvolge maggiormente la porzione più distale dell’arto e all’insorgenza appare tipicamente in un unico braccio o gamba, divenendo successivamente bilaterale.[35] La frequenza del tremore parkinsoniano è compresa tra i 4 e 6 hertz (cicli al secondo) ed è descritto come l’atto di “contare le monete” o come pill-rolling,[35][36] un termine che deriva dalla somiglianza tra il movimento nei pazienti e la tecnica utilizzata in farmaceutica per preparare manualmente le pillole.[36] La bradicinesia (lentezza dei movimenti) è un’altra caratteristica della malattia ed è associata a difficoltà in tutto il processo del movimento, dalla pianificazione alla iniziazione e, infine, all’esecuzione.[35] Il movimento sequenziale e simultaneo viene ostacolato.[35] La bradicinesia è il sintomo più invalidante nei primi stadi della malattia.[13] Queste manifestazioni comportano diversi problemi durante l’esecuzione delle attività quotidiane che richiedono un controllo fine dei movimenti, come la scrittura, il cucito o il vestirsi.[35] La valutazione clinica si basa su prove riguardanti operazioni simili.[13] La bradicinesia non è uguale per tutti i movimenti, alcuni pazienti risultano in grado di camminare con grandi difficoltà, ma tuttavia riescono ancora ad andare in bicicletta.[35] Generalmente gli individui che presentano bradicinesia, mostrano difficoltà minori se gli vengono forniti degli ausili.[35][37]
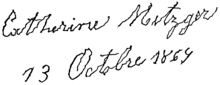
Grafia di una persona affetta da malattia di Parkinson, tratta da Lectures on the diseases of the nervous system di Jean-Martin Charcot (1879).
La rigidità e la resistenza al movimento degli arti è causata da una contrazione eccessiva e continua dei muscoli.[35] Nel parkinsonismo la rigidità può essere uniforme (a “tubo di piombo”) o a scatti (rigidità “a ruota dentata”).[35][13][38][39] La combinazione di tremore e l’aumento del tono muscolare, sono considerati l’origine della rigidità a ruota dentata.[40] La rigidità può essere associata a dolore articolare, tale dolore è una frequente manifestazione iniziale della malattia[35] Nelle fasi iniziali, la rigidità è spesso asimmetrica e tende a influenzare i muscoli del collo e delle spalle, rispetto ai muscoli del viso e degli arti.[41] L’instabilità posturale è tipica delle ultime fasi. Ciò comporta disturbi dell’equilibrio e frequenti cadute che possono causare fratture ossee.[35] L’instabilità è spesso assente nelle fasi iniziali, soprattutto nelle persone più giovani.[13] Fino al 40% dei pazienti possono andare incontro a cadute e circa il 10% cade settimanale, con un numero di cadute correlabile alla gravità della malattia.[35] La deambulazione avviene tipicamente mediante piccoli passi, strisciati, con un avvio molto problematico e spesso si apprezza il fenomeno della “festinazione”, cioè la progressiva accelerazione della camminata sino a cadere.[35] Vi possono essere disturbi della deglutizione, il linguaggio può divenire monotono, poco espressivo, lento (bradilalia)[35] la mimica facciale è scarsa e l’espressione impassibile. Anche la scrittura in un certo senso evolve nello stesso modo (micrografia parkinsoniana) con grafia che tende a rimpicciolirsi. Tuttavia, la gamma dei sintomi motori può essere molto più vasta.[35]
Sintomi neuropsichiatrici
Malattia di Parkinson può causare disturbi neuropsichiatrici che possono essere da lievi a gravi. Questi includono disturbi del linguaggio, della cognizione, dell’umore, del comportamento e del pensiero.[35] Disturbi cognitivi possono verificarsi nelle fasi iniziali della malattia e, talvolta, prima della diagnosi. La prevalenza di essi aumenta con la durata della malattia.[35][42] Il deficit cognitivo più comune è la disfunzione esecutiva, che può comprendere difficoltà nella pianificazione, nella flessibilità cognitiva, nel pensiero astratto, nell’avvio di azioni appropriate e nell’inibizione delle operazioni inappropriate. Le fluttuazioni dell’attenzione e il rallentamento della velocità cognitiva, sono ulteriori problemi a livello cognitivo. La memoria viene influenzata, in particolare nel ricordare le informazioni apprese. Tuttavia, appare un miglioramento quando il richiamo dei ricordi viene aiutato da stimoli.[42] Una persona con malattia di Parkinson ha da 2 a 6 volte il rischio di soffrire di demenza rispetto alla popolazione in generale.[35][42] La prevalenza della demenza aumenta con il decorso della malattia.[42] La demenza è associata con una forte riduzione della qualità della vita, sia nei pazienti che in chi li assiste. Inoltre, ciò comporta un aumento della mortalità e una maggiore probabilità che si renda necessaria un’assistenza infermieristica.[42] Alterazioni del comportamento e dell’umore sono più comuni nella malattia di Parkinson rispetto alla popolazione in generale. I problemi più frequenti sono la depressione[43], l’apatia e l’ansia.[35] Possono verificarsi difficoltà nel controllo degli impulsi, che possono portare all’abuso di farmaci, all’alimentazione compulsiva, all’ipersessualità, al gioco d’azzardo patologico. Questi aspetti sono stati correlati ai farmaci usati per gestire la malattia.[35][44] Sintomi psicotici, come allucinazioni o deliri, si verificano nel 4% dei pazienti e si presume che la causa principale sia un eccesso di dopamina secondario al trattamento, diventano infatti più comuni con l’aumentare dell’età e con l’assunzione di levodopa.[45][46]
Altri sintomi
Oltre ai sintomi cognitivi e motori, la malattia di Parkinson può compromettere altre funzioni dell’organismo. Problemi di sonno sono una caratteristica della malattia e possono essere aggravati dai farmaci.[35] I sintomi possono manifestarsi con sonnolenza diurna, disturbi del sonno nella fase REM o insonnia.[35] Le alterazioni del sistema nervoso autonomo possono portare a ipotensione ortostatica (pressione del sangue bassa in posizione eretta), pelle grassa e eccessiva sudorazione, incontinenza urinaria e alterata funzione sessuale.[35] La costipazione e i disturbi della motilità gastrica, possono essere abbastanza importanti, tanto da creare disagio e mettere in pericolo l’individuo.[47] La condizione comporta alterazioni nella vista, secchezza degli occhi, inseguimento oculare carente e movimenti saccadici (rapidi movimenti involontari di entrambi gli occhi, nella stessa direzione), difficoltà a dirigere lo sguardo verso l’alto e visione offuscata o doppia.[35][48] Modifiche nella percezione possono comprendere: alterazione dell’olfatto, sensazione di dolore e parestesie (formicolio e intorpidimento della pelle).[35] Tutti questi sintomi possono verificarsi anche per anni prima che vanga fatta la diagnosi della malattia.[35]
Diagnosi
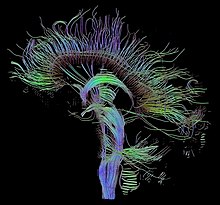
Ricostruzione trattografica delle connessioni neurali, grazie alla risonanza magnetica con imaging con tensore di diffusione.
Un medico può diagnosticare la malattia di Parkinson partendo dalla storia clinica e da un esame neurologico.[35] Al 2012, non esiste un test che identifichi chiaramente la malattia, ma scansioni tomografiche cerebrali sono a volte utilizzate per escludere patologie che potrebbero dare luogo a sintomi simili. L’osservazione di corpi di Lewy nel mesencefalo, in sede di autopsia, è solitamente considerata la prova che il paziente soffriva della malattia di Parkinson. Le linee guida consigliano di valutare periodicamente la diagnosi, poiché la progressione della malattia può far cambiare opinione su di essa.[35][49] Organizzazioni mediche hanno creato criteri per facilitare e standardizzare il processo diagnostico, soprattutto nelle fasi iniziali della malattia. I più conosciuti provengono dalla britannica Parkinson’s Disease Society Brain Bank e dalla statunitense National Institute of Neurological Disorders and Stroke.[35] I criteri del primo istituto citato richiedono la presenza di lentezza nei movimenti (bradicinesia) più rigidità, tremore a riposo o instabilità posturale. Le altre possibili cause di questi sintomi devono essere escluse. Infine, tre o più delle seguenti caratteristiche sono necessarie durante l’insorgenza o l’evoluzione: esordio unilaterale, tremore a riposo, progressione nel tempo, asimmetria dei sintomi motori, risposta alla levodopa per almeno cinque anni, decorso clinico di almeno dieci anni e verificarsi di discinesie indotte dall’assunzione eccessiva di levodopa.[35] La precisione di questi criteri diagnostici, valutati dopo autopsia, è del 75-90%, con gli specialisti in neurologia neurologi che hanno i numeri di diagnosi corrette più elevati.[35]
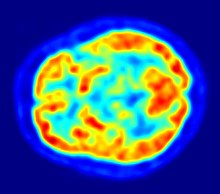
Esame PET mediante fluorodesossiglucosio di un cervello sano. Le aree più rosse riflettono l’assorbimento superiore del glucosio. Una diminuzione dell’attività nei gangli basali può aiutare nella diagnosi di morbo di Parkinson.
La tomografia computerizzata (TC) e la risonanza magnetica (MRI) del cervello di persone con malattia di Parkinson appaiono di solito normali.[50] Queste tecniche sono comunque utili per escludere altre malattie che possono essere cause secondarie del parkinsonismo, come i tumori vascolari, patologie dei gangli della base e idrocefalo.[50] Una tecnica particolare di risonanza magnetica, l’imaging con tensore di diffusione, è stata trovata utile nel discriminare tra parkinsonismo tipico e atipico, anche se il suo esatto valore diagnostico è ancora oggetto di studio.[50][51] Inoltre, sono utilizzate la risonanza magnetica funzionale e la spettroscopia a risonanza magnetica. Di recente introduzione vi è la sonografia transcranica, una nuova metodica che permette di studiare in modo non invasivo e a basso costo il parenchima dei nuclei della base e del mesencefalo. Tutto ciò con l’ausilio della finestra temporale.[52][53][54] La medicina nucleare permette uno studio accurato della patologia dal punto di vista anatomico e funzionale. Essa sfrutta l’uso di traccianti radioattivi iniettati nell’organismo, i quali vanno a depositarsi nei distretti corporei oggetto di studio, evidenziandone il metabolismo, e quindi in maniera diretta o indiretta, caratteristiche come la vitalità o l’attività. Essendo la malattia di Parkinson una patologia a carico del sistema dopaminergico, i traccianti sono diretti verso il trasportatore della dopamina e verso il trasportatore vescicolare delle monoamine di tipo 2 e verso l’enzima DOPA decarbossilasi. La posizione in cui i traccianti vanno a depositarsi vengono rilevati tramite PET[55] e SPECT.[56] Esempi di radiotraccianti utilizzabili sono: lo ioflupane (123I) (nome commerciale DaTSCAN) e iometopane (Dopascan) per la SPECT e il fluorodesossiglucosio (18F) per la PET.[50] Un modello sulla riduzione dell’attività dopaminergica nei gangli basali può aiutare nella diagnosi di malattia di Parkinson.[50]
Diagnosi differenziale
Altre cause che possono secondariamente produrre una sindrome parkinsoniana sono: la malattia di Alzheimer, l’ictus cerebrale e il parkinsonismo farmaco-indotto.[49] Nella diagnosi devono essere escluse sindromi come la paralisi sopranucleare progressiva e l’atrofia sistemica multipla.[35] Tassi di progressione veloci, precoce disfunzione cognitiva o instabilità posturale, tremore minimo o simmetrico all’esordio, possono indicare la presenza di una sindrome ulteriore, piuttosto che la malattia di Parkinson stessa.[57] Le forme genetiche sono di solito classificate come “malattia di Parkinson”, anche se i termini di “malattia familiare di Parkinson” e “parkinsonismo familiare” sono utilizzati per i soggetti con malattia autosomica dominante o recessiva.[13]
Terapia
Ad oggi, 2012, non esiste una cura per la malattia di Parkinson, ma il trattamento farmacologico, la chirurgia e la gestione multidisciplinare sono in grado di fornire sollievo ai sintomi. I farmaci principalmente utilizzati nel trattamento di sintomi motori sono la levodopa (di solito in combinazione con un inibitore della dopa-decarbossilasi e un inibitore delle COMT), gli agonisti della dopamina egli inibitori MAO-B (Inibitore della monoamino ossidasi).[58] La fase della malattia determina quale famiglia di farmaci sia più utile. Due fasi sono di solito distinte: una prima fase in cui l’individuo con la malattia ha già sviluppato qualche disabilità e per il quale vi è la necessità di un trattamento farmacologico, una seconda fase in cui in un individuo si sviluppano complicanze motorie legate all’utilizzo della levodopa.[58] Il trattamento nella fase iniziale ha come obiettivo un compromesso ottimale tra il buon controllo dei sintomi e gli effetti collaterali derivanti dalla valorizzazione della funzione dopaminergica. L’inizio del trattamento con levodopa (o L-DOPA) può essere ritardato utilizzando altri farmaci come gli inibitori MAO-B e gli agonisti della dopamina, nella speranza di ritardare la comparsa delle discinesie.[58] Nella seconda fase l’obiettivo è quello di ridurre sintomi. Quando i farmaci non sono più sufficienti a controllarli, la chirurgia e la stimolazione cerebrale profonda possono rivelarsi utili.[59] Nelle fasi finali della malattia, le cure palliative vengono offerte per migliorare la qualità di vita.[60]
Levodopa
| Per approfondire, vedi la voce Levodopa. |

La Levodopa è il trattamento più ampiamente usato fin dagli anni 70.[58] L-DOPA è convertito in dopamina nei neuroni dopaminergici mediante dopa decarbossilasi.[58] Poiché i sintomi motori sono prodotti da una mancanza di dopamina nella substantia nigra, la somministrazione di L-DOPA diminuisce temporaneamente i sintomi motori.[58] Solo il 5-10% dell’L-DOPA attraversa la barriera ematoencefalica. Il resto è spesso metabolizzato altrove in dopamina, provocando una serie di effetti collaterali tra cui nausea, discinesia e rigidità articolare.[58] La carbidopa e la benserazide sono inibitori della dopa decarbossilasi periferiche,[58] che aiutano a bloccare il metabolismo della L-DOPA, prima che raggiunga i neuroni dopaminergici, riducendo pertanto gli effetti collaterali e aumentando la biodisponibilità. Essi sono generalmente somministrati in preparazioni associate alla levodopa.[58] I preparati esistenti sono carbidopa/levodopa (co-careldopa) e benserazide/levodopa (co-beneldopa). La levodopa è stata correlata alla sindrome da disregolazione dopaminergica, che consiste in un uso eccessivo e compulsivo del farmaco.[44] Vi sono alcune versioni a rilascio controllato e lento di levodopa, tuttavia esse non hanno mostrato un maggiore controllo dei sintomi e delle complicanze motorie rispetto a preparazioni a rilascio immediato.[58][61] Il tolcapone inibisce l’enzima COMT, degradante la dopamina, prolungando gli effetti della levodopa.[58] Tuttavia, la sua utilità è limitata da effetti collaterali, come ad esempio i possibili danni al fegato.[58] Un farmaco altrettanto efficace, l’entacapone, non ha mostrato causare alterazioni significative della funzionalità epatica.[58] I preparati a base di levodopa, a lungo termine portano allo sviluppo di complicanze motorie caratterizzate da movimenti involontari. chiamati discenesie e fluttuazioni nella risposta al trattamento farmacologico.[58] In questo caso, un paziente affetto da malattia di Parkinson, può sperimentare dei periodi con buona risposta ai farmaci con alcuni sintomi (fase on) e periodi con nessuna risposta al trattamento e sintomi motori significativi (fase off).[58] Per questo motivo, le dosi di levodopa sono tenute il più basso possibile.[58] È pratica comune ritardare l’inizio della terapia con levodopa utilizzando alternative, come gli agonisti dopaminergici e gli inibitori della monoamino ossidasi.[58] Una strategia utilizzata in passato per ridurre le complicanze motorie era quella di sospendere il trattamento con L-DOPA per un certo tempo. Ora ciò è sconsigliato ora, dal momento che può portare a effetti collaterali pericolosi, come la sindrome neurolettica maligna.[58]
Agonisti dopaminergici
| Per approfondire, vedi la voce Agonisti dopaminergici. |

Strutture dei gangli basali nel trattamento del morbo di Parkinson. Modello degli effetti dei farmaci sui sintomi motori.
Numerosi agonisti della dopamina, che si legano ai recettori dopaminergici post-sinaptici del cervello hanno effetti simili a quelli della levodopa.[58] inizialmente venivano usati negli individui che accusano fluttuazioni on-off e discinesie, come terapia complementare alla levodopa. Ora sono utilizzati principalmente come terapia unica iniziale per i sintomi motori, con l’obiettivo di ritardare l’assunzione di levodopa e le sue complicazioni motorie.[58][62] Gli agonisti dopaminergici stimolano, con diversa specificità rispetto ai diversi tipi, i recettori per la dopamina. Si dividono in ergolinici (bromocriptina, pergolide, lisuride, cabergolina) e non ergolinici (pramipexolo, ropinirolo, apomorfina). Gli agonisti della dopamina producono significativi, anche se di solito lievi, effetti collaterali, tra cui sonnolenza, allucinazioni, insonnia, nausea e stipsi.[58] A volte gli effetti collaterali appaiono anche con una minima dose clinicamente efficace, che porta il prescrivente alla ricerca di un farmaco diverso.[58] Rispetto alla levodopa, gli agonisti della dopamina possono ritardare le complicanze motorie, ma sono meno efficaci nel controllare i sintomi.[58] Tuttavia, solitamente appaiono sufficienti per gestire i sintomi nei primi anni di malattia.[13] Essi tendono ad essere più costosi della levodopa.[13] Tali farmaci sono stati correlati a disturbi del controllo degli impulsi, come l’ipersessualità, l’alimentazione compulsiva e il gioco d’azzardo e lo shopping patologici, in maniera anche più importante rispetto alla levodopa.[44] Apomorfina, un agonista della dopamina, può essere utilizzato per ridurre le fasi off e la discinesia, nella malattia avanzata.[58] Viene somministrata attraverso iniezioni sottocutanee.[58] Dato che gli effetti secondari, come la confusione e le allucinazioni sono comuni, i pazienti che ricevono l’apomorfina devono essere attentamente monitorati.[58] Recentemente sono stati trovati due agonisti della dopamina che vengono somministrati attraverso cerotti (lisuride e rotigotina) e risultano essere utili nei pazienti nella fase iniziale della malattia, mentre vi sono ancora degli studi alla fase preliminare riguardo alla loro efficacia nei pazienti in stato avanzato.[58]
Inibitori della monoamino ossidasi
| Per approfondire, vedi la voce Inibitore della monoamino ossidasi. |

Struttura molecolare della selegilina, uno degli inibitori della monoamino ossidasi utilizzati nel trattamento della malattia.
Gli inibitori della monoamino ossidasi (inibitori MAO-B), selegilina e rasagilina, sono in grado di aumentare il livello di dopamina nei gangli della base, bloccandone il suo metabolismo. Essi bloccano la deaminazione ossidativa delle amine endogene catalizzata dalle monoaminossidasi mitocondriali. La riduzione della attività della monoamino ossidasi, comporta un aumento di L-DOPA nello striato.[58] Come gli agonisti della dopamina, gli inibitori MAO-B sono utilizzati in monoterapia per migliorare i sintomi motori e ritardare la necessità di assumere levodopa nella malattia precoce, ma producono effetti più negativi e sono meno efficaci rispetto alla levodopa. Vi sono pochi studi sulla loro efficacia in fase avanzata, anche se i risultati suggeriscono che essi sono utili per ridurre le fluttuazioni tra le fasi on e off.[58] Uno studio iniziale ha indicato che la selegilina, in associazione con levodopa, aumenta il rischio di morte, ma ciò è stato in seguito smentito.[58]
Altri farmaci
Altri farmaci, come l’amantadina e gli anticolinergici, possono essere utili come trattamento dei sintomi motori. Tuttavia, le prove a loro sostegno mancano di qualità e ciò comporta che non siano considerati trattamenti di prima scelta.[58] Oltre ai sintomi motori, la malattia di Parkinson è accompagnata da una vasta gamma di sintomi. Un certo numero di farmaci sono stati utilizzati per il trattamento di alcuni di questi problemi.[63] Ne sono un esempio l’uso della clozapina nella psicosi, degli inibitori della colinesterasi per la demenza e il modafinil per la sonnolenza diurna.[63][64] Una meta-analisi del 2010, ha riscontrato che l’uso di farmaci anti-infiammatori non steroidei (tranne il paracetamolo e l’aspirina), sono stati correlati ad almeno il 15% di una minore incidenza di sviluppo della malattia di Parkinson.[65]
Terapia chirurgica

Posizionamento di un elettrodo nel cervello. La testa è stabilizzata con una tecnica utilizzata nella chirurgia stereotassica.
Una volta, trattare i sintomi motori con un intervento chirurgico, era una pratica comune, ma dal momento che venne scoperta la levodopa, il numero di interventi diminuì.[66] Gli studi degli ultimi decenni hanno portato a grandi miglioramenti nelle tecniche chirurgiche, con la conseguenza che la chirurgia è nuovamente utilizzata nelle persone sofferenti la malattia di Parkinson e per le quali la terapia farmacologica non è più sufficiente.[66] Attualmente la tecnica più utilizzata è la chirurgia stereotassica che permette di trattare punti in profondità nel parenchima cerebrale con precisione millimetrica, grazie all’ausilio di dispositivi radiologici. Il trattamento chirurgico per la condizione, può essere distinto in due gruppi principali: stimolazione cerebrale profonda (Deep Brain Stimulation, DBS) o intervento lesionale. I settori di intervento sono il talamo, il globo pallido o il nucleo subtalamico.[66] La stimolazione cerebrale profonda (DBS) è il trattamento chirurgico più comunemente utilizzato e permette una buona remissione clinica e una significativa riduzione della dipendenza da levodopa.[67] Esso comporta l’impianto di un dispositivo medico, chiamato pacemaker cerebrale, che invia impulsi elettrici a zone specifiche del cervello. La DBS è raccomandata per i pazienti con Parkinson che soffrono di forte tremore che non viene adeguatamente controllato da farmaci o in coloro che sono intolleranti al trattamento farmacologico.[59] Uno studio pubblicato nel Journal of the American Medical Association ed effettuato su un campione di 225 malati, ha evidenziato, nel 71% dei casi, decisivi miglioramenti nei movimenti e nella diminuzione dei tremori in seguito alla DBS, rispetto al 30% che prendeva solo farmaci.[68][69] Altre, ma meno comuni, terapie chirurgiche comportano la creazione di lesioni in specifiche aree sottocorticali (una tecnica nota come pallidotomia, nel caso che la lesione sia prodotta nel globo pallido).[66]
Riabilitazione
Nonostate gli studi al riguardo siano scarsi e di bassa qualità, l’esperienza fornisce alcune prove che i problemi di linguaggio e di mobilità sono in grado di migliorare grazie alla riabilitazione.[70][71] L’esercizio fisico regolare, con o senza fisioterapia, può essere utile per mantenere e migliorare la mobilità, la flessibilità, la forza, l’andatura e la qualità della vita.[71] Tuttavia, quando un programma di esercizio viene svolto sotto la supervisione di un fisioterapista, si possono riscontrare maggiori miglioramenti sia nella mobilità, che nelle funzioni mentali ed emotive, che nelle attività quotidiane della vita.[72] Per migliorare la capacità di movimento nei pazienti che presentano rigidità, sono stati proposti esercizi e tecniche di rilassamento, come dolci dondolii, che aiutano a diminuire l’eccessiva tensione muscolare. Altre efficaci tecniche includono lenti movimenti di rotazione degli arti e del tronco, la respirazione diaframmatica e tecniche di meditazione.[73] Per quanto riguarda la deambulazione, i fisioterapisti possono proporre una serie di strategie per migliorare la mobilità e la sicurezza funzionale. Queste puntano a migliorare la velocità di andatura, la lunghezza del passo, il movimento del tronco e del braccio.[74] Gli esercizi studiati per rafforzare la muscolatura si sono dimostrati utili per migliorare la funzionalità motoria nei pazienti con debolezza muscolare e debolezza relativa all’inattività. Tuttavia, i rapporti mostrano una significativa interazione tra la forza e il momento in cui sono stati assunti i farmaci. Pertanto, si raccomanda che i pazienti eseguano gli esercizi da 45 minuti a un’ora dopo aver assunto la terapia, ovvero quando il paziente è al meglio.[75] Inoltre, a causa della postura flessa in avanti e delle disfunzioni respiratorie presenti nella fase avanzata della malattia, gli esercizi di respirazione profonda diaframmatica sono utili per migliorare la mobilità della parete toracica e della funzionalità vitale.[76] L’attività fisica può migliorare la stitichezza.[47] Uno dei trattamenti più ampiamente praticati per i disturbi del linguaggio associati al morbo di Parkinson è la terapia vocale con il metodo Lee Silverman (LSVT).[70][77] La Logopedia e in particolare la LSVT possono migliorare il linguaggio.[70] La terapia occupazionale mira a promuovere la salute e la qualità della vita, aiutando le persone con la malattia a compiere molte delle loro attività della vita quotidiana il più autonomamente possibile.[70] Vi sono stati pochi studi sull’efficacia della terapia occupazionale, nonostante ciò, vi sono anche se vi sono prove che essa possa migliorare le capacità motorie e la qualità della vita dei pazienti affetti da malattia di Parkinson.[70][78]
Alimentazione
I muscoli e i nervi che controllano la digestione possono essere influenzati dalla malattia, con conseguente costipazione e gastroparesi (il cibo rimane nello stomaco per un periodo di tempo più lungo del normale).[47] Una alimentazione equilibrata, sulla base di periodiche valutazioni nutrizionali, è consigliata e deve essere finalizzata ad evitare la perdita o il guadagno di peso e a ridurre al minimo le conseguenze delle disfunzioni gastrointestinali.[47] Con l’avanzare della malattia, può comparire difficoltà disfagia ossia la difficoltà nella deglutizione. In questi casi può essere utile usare addensanti per l’assunzione di liquidi e assumere una postura eretta quando si mangia, entrambe le misure riducono il rischio di soffocamento. Nei casi più gravi si può ricorrere alla gastrostomia per fornire il cibo direttamente nello stomaco.[47] Il farmaco levodopa e le proteine utilizzano, in concorrenza, lo stesso sistema di trasporto nell’intestino e nella barriera emato-encefalica.[47] Questo comporta che, se assunti insieme, l’efficacia del farmaco appare ridotta.[47] Pertanto, quando si fa uso di levodopa, si sconsiglia il consumo eccessivo di proteine e viene raccomandata una equilibrata dieta mediterranea. Negli stadi avanzati, l’assunzione supplementare di prodotti ipoproteici, come pane o pasta, viene consigliata per ragioni analoghe.[47] Per minimizzare l’interazione con le proteine, la levodopa deve essere assunta 30 minuti prima dei pasti.[47]
Le cure palliative
Il ricorso alle cure palliative è spesso richiesto nelle fasi finali della malattia, quando tutte le altre strategie di trattamento sono diventate inefficaci. Lo scopo delle cure palliative è quello di ottimizzare la qualità della vita, sia per il paziente che per tutti quelli che lo circondano. Alcuni obbiettivi centrali delle cure palliative sono: cure adeguate nella propria comunità, riduzione o sospensione dell’assunzione dei farmaci per ridurre gli effetti collaterali, prevenzione delle piaghe da decubito nei pazienti allettati, supporto per il paziente e per le persone a lui vicine.[60]
Altri trattamenti
È stato dimostrato che la stimolazione magnetica transcranica migliora temporaneamente la discinesia indotta dalla levodopa.[79] La sua utilità nel trattamento della malattia di Parkinson è un argomento di ricerca ancora aperto,[80] anche se studi recenti non hanno dimostrato alcun effetto.[81] Diversi nutrienti sono stati proposti come possibili trattamenti, ma non vi sono prove che le vitamine o additivi alimentari siano in grado di migliorare i sintomi.[82] Non vi sono prove a sostegno che l’agopuntura e la pratica del Qigong o del T’ai chi, abbiano alcun effetto sul decorso della malattia o sulla presentazione dei sintomi. Tuttavia, sono necessarie ulteriori ricerche sul T’ai chi quando viene utilizzato al fine di migliorare la capacità di equilibrio.[83][84][85] La mucuna pruriens e la vicia faba sono fonti naturali di levodopa e sono assunte da molte persone con la malattia. Sebbene abbiano dimostrato una certa efficacia in studi clinici,[86] la loro ingestione non è esente da rischi. Sono state, infatti, riportate delle reazioni avverse letali, come la sindrome neurolettica maligna.[87][88]
Prognosi

Disability-adjusted life yearper malattia di Parkinson per 100.000 abitanti nel 2004
|
██ nessun dato ██ < 5 ██ 5–12.5 ██ 12.5–20 ██ 20–27.5 ██ 27.5–35
|
██ 35–42.5 ██ 42.5–50 ██ 50–57.5 ██ 57.5–65 ██ 65–72.5 ██ 72.5–80 ██ > 80
|
La malattia di Parkinson progredisce sempre con il tempo. La scala di Hoehn e Yahr, che definisce cinque stadi di progressione, è comunemente usata per stimare lo stadio della malattia.[89] I sintomi motori, se non trattati, avanzano aggressivamente nelle fasi iniziali della malattia e più lentamente in seguito. Se non trattati, si può prevedere che i pazienti vadano incontro ad una perdita della deambulazione indipendente dopo una media di otto anni e di essere costretti a letto dopo dieci anni.[90] Tuttavia, è raro, al giorno d’oggi, trovare persone che non ricevano un trattamento. I farmaci hanno migliorato la prognosi dei sintomi motori, mentre allo stesso tempo vi è una nuova fonte di disabilità a causa degli effetti indesiderati della levodopa, che si verificano dopo anni di utilizzo.[90] Per le persone che assumono levodopa, il tempo di progressione dei sintomi dall’esordio ad una fase di completa non autosufficienza, può essere di oltre i 15 anni.[90] Tuttavia, è difficile prevedere quale decorso prenderà la malattia per un dato paziente.[90] L’età è il miglior predittivo della progressione della malattia.[32] Il deficit cognitivo è più frequente in coloro che hanno più di 70 anni di età all’insorgenza dei sintomi.[32] Dal momento che le attuali terapie sono in grado di migliorare i sintomi motori, la disabilità è principalmente collegata alle caratteristiche non-motorie della malattia.[32] Tuttavia, il rapporto tra la progressione della malattia e la disabilità non è lineare. Inizialmente la disabilità è legata ai sintomi motori,[90] con l’avanzare della malattia essa risulterà più correlata con i sintomi che non rispondono adeguatamente al trattamento farmacologico, come ad esempio la deglutizione, la difficoltà di parola e di equilibrio. Inoltre vi è da tener conto delle complicanze relative al movimento, che appaiono nel 50% degli individui dopo 5 anni di utilizzo di levodopa.[90] Infine, dopo dieci anni, la maggior parte dei pazienti sperimenta dei disturbi autonomici, disturbi del sonno, alterazioni dell’umore e declino cognitivo.[90] Tutti questi sintomi, in particolare il declino cognitivo, aumentano notevolmente la disabilità.[32][90]
Scala di Hoehn e Yahr
La scala di Hoehn e Yahr è usata comunemente per descrivere i sintomi della progressione della malattia di Parkinson. È stata originariamente pubblicata nel 1967 sulla rivista Neurology da Melvin Yahr e Margaret Hoehn e comprendeva gli stadi da 1 a 5. Da allora, una scala modificata è stata proposta, con l’aggiunta degli stadi 1,5 e 2,5 per descrivere il decorso intermedio della malattia.[89][91]
| Stadio | Scala di Hoehn e Yahr | Scala di Hoehn e Yahr modificata |
|---|---|---|
| 1 | Coinvolgimento unilaterale, solitamente con solo una minima o nessuna disabilità funzionale | Solo coinvolgimento unilaterale |
| 1.5 | – | Coinvolgimento unilaterale e assiale |
| 2 | Coinvolgimento bilaterale o mediano senza compromissione dell’equilibrio | Coinvolgimento bilaterale senza compromissione dell’equilibrio |
| 2.5 | – | Lieve coinvolgimento bilaterale senza recupero sul test a trazione |
| 3 | Coinvolgimento bilaterale da medio a moderato; alcune difficoltà posturali; fisicamente indipendente | |
| 4 | Malattia gravemente debilitante, ancora in grado di camminare o stare in piedi senza assistenza | Grave disabilità; ancora in grado di camminare o stare in piedi senza assistenza |
| 5 | Costretto a letto o sulla sedi a rotelle | Costretto a letto o sulla sedi a rotelle |
Mortalità
L’aspettativa di vita dei malati di Parkinson appare ridotta.[90] I tassi di mortalità sono circa il doppio di quelli delle persone non affette.[90] Il declino cognitivo e la demenza, l’esordio in vecchiaia, uno stato di malattia più avanzato e la presenza di problemi nella deglutizione, sono tutti fattori che aumentano il rischio di mortalità. D’altra parte, una malattia caratterizzata principalmente da tremore rispetto alla rigidità, prevede una sopravvivenza più lunga.[90] La morte da polmonite ab ingestis è due volte più frequente nei soggetti con malattia di Parkinson rispetto alla popolazione sana.[90]
Società e cultura
Costi

Muhammad Ali, nel 2006 all’età di 64. Iniziò mostrare segni di parkinsonismo dall’età di 38.
La malattia di Parkinson costituisce un costo molto elevato per la società, ma un valore preciso di ciò è difficile da determinare per via di problemi metodologici nella stima e per le differenze che esistono tra i vari paesi.[92] Il costo annuale nel Regno Unito è stimato tra i 449 milioni e i 3,3 miliardi di sterline, mentre il costo per paziente per anno negli Stati Uniti si aggira introno ai $ 10.000, per un totale di circa 23 miliardi di dollari.[92] La quota maggiore del costo diretto viene dai ricoveri e dai soggiorni nelle case di cura, mentre la parte proveniente dai farmaci è sostanzialmente inferiore.[92] Anche i costi indiretti sono elevati, per via della riduzione della produttività e degli oneri che ricadono sui caregiver, ovvero su chi assiste i pazienti.[92] Oltre ai costi economici, la malattia riduce la qualità della vita di coloro che ne soffrono e di chi li assiste.[92]
Patrocini
L’11 aprile, l’anniversario della nascita di di James Parkinson, è stato designato come il giorno dedicato alla malattia.[5][93] Un tulipano rosso è stato scelto, nel 2005, dalle organizzazioni internazionali come il simbolo della malattia.[93] Tra le più importanti organizzazioni di rappresentanza e difesa vi sono le statunitensi National Parkinson Foundation, che ha fornito più di $ 155 milioni per la cura, la ricerca e i servizi di supporto dal 1982,[94] la Parkinson Disaese Foundation, che ha fornito più di $ 90 milioni per la ricerca e $ 37 milioni per programmi di educazione e sensibilizzazione fin dalla sua fondazione, avvenuta nel 1957 per opera di William Black,[95][96] l’American Parkinson Disease Association, fondata nel 1961,[97] e l’Associazione Europea per il Morbo di Parkinson, fondata nel 1992.[98]
Casi famosi
La rivelazione dell’attore Michael J. Fox di essere affetto da malattia di Parkinson, ha notevolmente aumentato la consapevolezza pubblica di essa. A Fox è stata diagnosticata nel 1991, quando aveva 30 anni, ma la sua condizione è stata tenuta nascosta per sette anni.[99] L’attore ha scritto due autobiografie incentrate sulla sua lotta contro la malattia.[100] La Michael J. Fox Foundation mira a sviluppare una cura per il morbo di Parkinson. Negli ultimi anni è stata l’organizzazione principale nella raccolta fondi negli Stati Uniti per la malattia di Parkinson, fornendo 140 milioni di dollari di finanziamento tra il 2001 e il 2008.[100] Fox è stato nominato, nel 2007, tra le 100 persone “il cui potere, talento o esempio morale stanno trasformando il mondo” secondo la rivista Time,[99] e ha ricevuto la Laurea honoris causa in medicina, dal Karolinska Institutet, per i suoi contributi alla ricerca nella malattia di Parkinson.[101] Una fondazione che sostiene la ricerca di Parkinson, puntando sulla qualità della vita dei pazienti, è stata fondata nel 2004 dal ciclista professionista e olimpico Davis Phinney, a cui a 40 anni è stata diagnosticata la malattia.[102] L’obiettivo della The Davis Phinney Foundation è aiutare le persone con la malattia a vivere bene, fornendo loro informazioni presidi e supporto.[103][104] Muhammad Ali è stato definito il “più famoso paziente con Parkinson al mondo”.[105] Al momento della diagnosi aveva 42 anni, anche se aveva iniziato a presentare dei sintomi già all’età di 38 anni.[106] È tuttora incerto che si tratti di malattia di Parkinson o di una sindrome parkinsoniana causata dalla boxe.[106][107]
Stato della ricerca
Ci sono poche possibilità che in un breve lasso di tempo vengano introdotti nuovi trattamenti rivoluzionari per la malattia di Parkinson.[108] Gli attuali campi di ricerca includono nuovi studi su modelli animali, sulle potenzialità della terapia genica, sul trapianto di cellule staminali e sugli agenti neuroprotettivi.[32]
Modelli animali
In natura, la malattia di Parkinson non si verifica in specie diverse dagli esseri umani. Cavie animali che mostrano alcune caratteristiche della malattia sono utilizzate nella ricerca. La comparsa dei sintomi parkinsoniani, avvenuta nei primi anni 90, in un gruppo di tossicodipendenti che avevano consumato una partita di oppiacei contaminati da MPPP, ha portato alla scoperta dell’MPTP come un agente causale della sindrome parkinsoniana nei primati, nonché in gli esseri umani.[109] Altri esperimenti incentrati su tossine hanno visto impiegare l’insetticida Rotenone, il diserbante Paraquat e il fungicida Maneb.[110] Queste prove sono state principalmente fatte su primati. Inoltre, sono stati impiegati particolari specie di roditori transgenici che riproducono i vari aspetti della malattia di Parkinson.[111]
Terapia genica
La terapia genica comporta l’uso di virus non infettivi per portare un gene in una parte del cervello. Il virus con il gene viene iniettato in una zona precisa del cervello, il nucleo subtalamico, che regola il circuito motorio. Il gene serve per produrre il neurotrasmettitore GABA che è deficitario nei pazienti affetti da Parkinson. Iniettando il gene per il GABA all’interno del cervello, i ricercatori hanno tentato di stimolare la produzione del neurotrasmettitore per normalizzare la funzione del circuito motorio.[32][112] Nel 2010 vi erano quattro studi clinici che avevano utilizzato la terapia genica nella malattia di Parkinson.[32] Non vi sono stati importanti effetti negativi in questi studi, anche se l’utilità clinica della terapia genica è ancora da determinare.[32] Un ulteriore risultato positivo è stato riportato nel 2011.[113] Altri promettenti recenti ricerche indicano la possibilità di usare tecniche di ingegneria genetica per “infettare” opportunamente i mitocondri di cellule dopaminergiche di topi con una proteina (beta 2.7) in grado di proteggere gli stessi dall’insulto e in definitiva rendendo più resistenti le stesse cellule al danno apoptotico.[114]
Trattamenti neuroprotettivi

Alcuni composti chimici, come il fattore di crescita neurotrofico derivato dalle cellule gliali, sono stati proposti come neuroprotettivi per la malattia di Parkinson. Tuttavia la loro efficacia non è stata ancora provata.
Studi su trattamenti neuroprotettivi sono sono in prima linea nella ricerca sulla malattia di Parkinson. Sono state proposte molecole diverse come potenziali trattamenti.[32] Tuttavia, nessuna di loro si è definitivamente dimostrata capace di ridurre la degenerazione.[32] Il farmaco neuroprotettivo più conosciuto e utilizzato è la selegilina (Deprenyl). La selegilina è un inibitore irreversibile della MAO-B che ha un effetto antiossidante, neurotrofico e antiapoptotico.[115] Ulteriori agenti attualmente sotto studio sono gli anti-apoptotici (omigapil, CEP-1347), l’acido glutammico, gli inibitori delle monoaminossidasi (la rasagilina e la già citata selegilina), farmaci favorenti la funzione mitocondriale (coenzima Q10 e la creatina), i calcio-antagonisti (isradipina) e il fattore di crescita neurotrofico derivato dalle cellule gliali.[32] La ricerca preclinica si rivolge anche alla alfa-sinucleina.[108] Un vaccino che inneschi il sistema immunitario umano a distruggere l’alfa-sinucleina, il PD01A (sviluppato dalla società austriaca, Affiris), è entrato negli studi clinici sugli esseri umani.[116]
Terapia con cellule staminali
Fin dal 1980, sono stati tentati impianti di vari tessuti biologici nella substantia nigra nella speranza che esse possano riprendere la produzione di dopamina.[32] Anche se alcuni studi iniziali hanno considerato la tecnica come promettente, studi più recenti tuttavia non hanno dimostrato alcun benenficio a lungo termine.[32] Un problema significativo è stato il rilascio eccessivo di dopamina da parte del tessuto trapiantato, con conseguenti distonie.[117] I trapianti di cellule staminali sono oggetto di importanti ricerche che hanno già presentato alcuni risultati positivi. La scoperta che tali celluel, se stimolate in vitro con il prodotto del gene NURR1 si differenziavano in cellule dopaminergiche, e che queste, se introdotte per via stereotassica nel cervello di ratti affetti da malattia di Parkinson ne rallentavano la progressione fino all’arresto, ha aperto orizzonti rivoluzionari nel trattamento della malattia.[118][32][119] Tuttavia, l’utilizzo di cellule staminali embrionali è controverso da un punto di vista etico.[32] È stato perciò proposto che di incentrare la ricerca sull’utilizzo delle cellule staminali pluripotenti indotte.[32]
Progetti informatici di calcolo distribuito
L’iniziativa Folding@home, un progetto informatico di calcolo distribuito, si propone di migliorare la comprensione della malattia di Parkinson, sfruttando la potenza di calcolo dei personal computer dei volontari.[120]
Note
- ^ Il termine morbo, dal latino Mòrbus, “malattia che conduce a morte”, è stato storicamente utilizzato per indicare le malattie a decorso fatale, soprattutto perché sconosciute e quindi incurabili. Attualmente è un vocabolo in via di abbandono sia per rispetto del malato, sia perché di molte malattie è stata trovata l’origine e la cura.
- ^ a b c García Ruiz PJ (dicembre 2004). Prehistoria de la enfermedad de Parkinson. Neurologia 19 (10): 735–7 (in Spanish; Castilian). PMID 15568171.
- ^ a b Lanska DJ (2010). Chapter 33: the history of movement disorders. Handb. Clin. Neurol. 95: 501–46. DOI:10.1016/S0072-9752(08)02133-7. PMID 19892136.
- ^ Koehler PJ, Keyser A (settembre 1997). Tremor in Latin texts of Dutch physicians: 16th–18th centuries. Mov. Disord. 12 (5): 798–806. DOI:10.1002/mds.870120531. PMID 9380070.
- ^ a b c d e f g h Lees AJ (settembre 2007). Unresolved issues relating to the shaking palsy on the celebration of James Parkinson’s 250th birthday. Mov. Disord. 22 (Suppl 17): S327–34. DOI:10.1002/mds.21684. PMID 18175393.
- ^ Louis ED (novembre 1997). The shaking palsy, the first forty-five years: a journey through the British literature. Mov. Disord. 12 (6): 1068–72. DOI:10.1002/mds.870120638. PMID 9399240.
- ^ a b c Fahn S (2008). The history of dopamine and levodopa in the treatment of Parkinson’s disease. Mov. Disord. 23 (Suppl 3): S497–508. DOI:10.1002/mds.22028. PMID 18781671.
- ^ a b c Schulz-Schaeffer WJ (agosto 2010). The synaptic pathology of alpha-synuclein aggregation in dementia with Lewy bodies, Parkinson’s disease and Parkinson’s disease dementia. Acta Neuropathol. 120 (2): 131–43. DOI:10.1007/s00401-010-0711-0. PMID 20563819.
- ^ Guridi J, Lozano AM (novembre 1997). A brief history of pallidotomy. Neurosurgery 41 (5): 1169–80; discussion 1180–3. DOI:10.1097/00006123-199711000-00029. PMID 9361073.
- ^ Hornykiewicz O (2002). L-DOPA: from a biologically inactive amino acid to a successful therapeutic agent. Amino Acids 23 (1–3): 65–70. DOI:10.1007/s00726-001-0111-9. PMID 12373520.
- ^ Coffey RJ (marzo 2009). Deep brain stimulation devices: a brief technical history and review. Artif. Organs 33 (3): 208–20. DOI:10.1111/j.1525-1594.2008.00620.x. PMID 18684199.
- ^ a b c d e f g h i j k l m n o de Lau LM, Breteler MM (June 2006). Epidemiology of Parkinson’s disease. Lancet Neurol. 5 (6): 525–35. DOI:10.1016/S1474-4422(06)70471-9.
- ^ a b c d e f g h i Samii A, Nutt JG, Ransom BR (May 2004). Parkinson’s disease. Lancet 363 (9423): 1783–93. DOI:10.1016/S0140-6736(04)16305-8.
- ^ Tanner CM, Kamel F, Ross GW, et al. (January 2011). Rotenone, Paraquat and Parkinson’s Disease. Environ Health Perspect 119 (6): 866–72. DOI:10.1289/ehp.1002839.
- ^ a b Neurologic disorders in IOM (Institute of Medicine) (a cura di), Veterans and Agent Orange: Update 2008, Washington D.C., The National Academies press, 2009, 510–45. ISBN 0-309-13884-1
- ^ a b Stern, MB. (1991). Head trauma as a risk factor for Parkinson’s disease.. Mov Disord 6 (2): 95-7. DOI:10.1002/mds.870060202. PMID 2057017.
- ^ Bhidayasiri, R. (Jun 2012). Boxing and Parkinson disease: a link or a myth? An 18F-FDOPA PET/CT study in retired Thai traditional boxers.. Parkinsonism Relat Disord 18 (5): 694-6. DOI:10.1016/j.parkreldis.2012.01.010. PMID 22321864.
- ^ a b Lolekha, P. (Sep 2010). Prevalence and risk factors of Parkinson’s disease in retired Thai traditional boxers.. Mov Disord 25 (12): 1895-901. DOI:10.1002/mds.23210. PMID 20669292.
- ^ Chaudhuri, KR. (Nov 1995). Magnetic resonance spectroscopic study of parkinsonism related to boxing.. J Neurol Neurosurg Psychiatry 59 (5): 561-2. PMID 8530957.
- ^ Campdelacreu, J. (Jun 2012). Parkinson disease and Alzheimer disease: environmental risk factors.. Neurologia. DOI:10.1016/j.nrl.2012.04.001. PMID 22703631.
- ^ Gao, X. (Oct 2012). Age, statin use, and the risk for incident Parkinson disease-reply.. Arch Neurol 69 (10): 1381. DOI:10.1001/archneurol.2012.2032. PMID 23044597.
- ^ Latoo, J. (Jun 2012). Depression in Parkinson’s disease: diagnosis and management.. Br J Hosp Med (Lond) 73 (6): 331-4. PMID 22875323.
- ^ Parkinson: esposizione a solvente chimico aumenta 6 volte rischio. URL consultato in data 17-11-2011.
- ^ Costa J, Lunet N, Santos C, Santos J, Vaz-Carneiro A (2010). Caffeine exposure and the risk of Parkinson’s disease: a systematic review and meta-analysis of observational studies. J. Alzheimers Dis. 20 (Suppl 1): S221–38. DOI:10.3233/JAD-2010-091525.
- ^ Góngora-Alfaro JL (2010 Feb 16-28). Caffeine as a preventive drug for Parkinson’s disease: epidemiologic evidence and experimental support. Rev Neurol 50 (4): 221–9 (in Spanish).
- ^ Quik M, Huang LZ, Parameswaran N, Bordia T, Campos C, Perez XA (2009-10-01). Multiple roles for nicotine in Parkinson’s disease. Biochem Pharmacol 78 (7): 677–85. DOI:10.1016/j.bcp.2009.05.003.
- ^ Castagnoli K, Murugesan T (2004 Jan). Tobacco leaf, smoke and smoking, MAO inhibitors, Parkinson’s disease and neuroprotection; are there links?. Neurotoxicology 25 (1–2): 279–91. DOI:10.1016/S0161-813X(03)00107-4.
- ^ a b c d e f g h Obeso JA, Rodríguez-Oroz MC, Benitez-Temino B, et al. (2008). Functional organization of the basal ganglia: therapeutic implications for Parkinson’s disease. Mov. Disord. 23 (Suppl 3): S548–59. DOI:10.1002/mds.22062.
- ^ a b c d e f g Davie CA (2008). A review of Parkinson’s disease. Br. Med. Bull. 86 (1): 109–27. DOI:10.1093/bmb/ldn013.
- ^ a b c Dickson DV, op. cit., pp. 271–283.
- ^ Jubault T, Brambati SM, Degroot C, et al. (2009). Regional brain stem atrophy in idiopathic Parkinson’s disease detected by anatomical MRI. PLoS ONE 4 (12): e8247. DOI:10.1371/journal.pone.0008247.
- ^ a b c d e f g h i j k l m n o p q r s Obeso JA, Rodriguez-Oroz MC, Goetz CG, et al. (May 2010). Missing pieces in the Parkinson’s disease puzzle. Nat. Med. 16 (6): 653–61. DOI:10.1038/nm.2165.
- ^ Hirsch EC (December 2009). Iron transport in Parkinson’s disease. Parkinsonism Relat. Disord. 15 (Suppl 3): S209–11. DOI:10.1016/S1353-8020(09)70816-8.
- ^ a b c d e f g h i Lesage S, Brice A (April 2009). Parkinson’s disease: from monogenic forms to genetic susceptibility factors. Hum. Mol. Genet. 18 (R1): R48–59. DOI:10.1093/hmg/ddp012.
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab ac ad ae af ag ah ai aj ak Jankovic J (April 2008). Parkinson’s disease: clinical features and diagnosis. J. Neurol. Neurosurg. Psychiatr. 79 (4): 368–76. DOI:10.1136/jnnp.2007.131045.
- ^ a b Cooper G, Eichhorn G, Rodnitzky RL, Parkinson’s disease in Conn PM (a cura di), Neuroscience in medicine, Totowa, NJ, Humana Press, 2008, 508–512. ISBN 978-1-60327-454-8
- ^ Rodriguez-Oroz MC, Jahanshahi M, Krack P, et al. (December 2009). Initial clinical manifestations of Parkinson’s disease: features and pathophysiological mechanisms. Lancet Neurol. 8 (12): 1128–39. DOI:10.1016/S1474-4422(09)70293-5.
- ^ Banich MT, Compton RJ, Motor control in Cognitive neuroscience, Belmont, CA, Wadsworth, Cengage learning, 2011, 108–44. ISBN 0-8400-3298-6
- ^ Oxford Handbook of Clinical Medicine, Oxford University Press, 2007-01-04, pp. 486. ISBN 978-0-19-856837-7
- ^ Fung VSC, Thompson PD, Rigidity and spasticity in Tolosa E, Jankovic JJ (a cura di), Parkinson’s disease and movement disorders, Hagerstown, MD, Lippincott Williams & Wilkins, 2007, 504–13. ISBN 0-7817-7881-6
- ^ O’Sullivan & Schmitz, op. cit., pp. 856-857.
- ^ a b c d e Caballol N, Martí MJ, Tolosa E (September 2007). Cognitive dysfunction and dementia in Parkinson disease. Mov. Disord. 22 (Suppl 17): S358–66. DOI:10.1002/mds.21677.
- ^ De Leo, op. cit., p. 323.
- ^ a b c Ceravolo R, Frosini D, Rossi C, Bonuccelli U (December 2009). Impulse control disorders in Parkinson’s disease: definition, epidemiology, risk factors, neurobiology and management. Parkinsonism Relat. Disord. 15 (Suppl 4): S111–5. DOI:10.1016/S1353-8020(09)70847-8.
- ^ Shergill SS, Walker Z, Le Katona C (October 1998). A preliminary investigation of laterality in Parkinson’s disease and susceptibility to psychosis. J. Neurol. Neurosurg. Psychiatr. 65 (4): 610–1. DOI:10.1136/jnnp.65.4.610.
- ^ Friedman JH (June 2010). Parkinson’s disease psychosis 2010: A review article. Parkinsonism Relat. Disord. 16 (9): 553–60. DOI:10.1016/j.parkreldis.2010.05.004.
- ^ a b c d e f g h i Barichella M, Cereda E, Pezzoli G (October 2009). Major nutritional issues in the management of Parkinson’s disease. Mov. Disord. 24 (13): 1881–92. DOI:10.1002/mds.22705.
- ^ Armstrong RA (March 2008). Visual signs and symptoms of Parkinson’s disease. Clin. Exp. Optom. 91 (2): 129–38. DOI:10.1111/j.1444-0938.2007.00211.x.
- ^ a b Diagnosing Parkinson’s Disease in The National Collaborating Centre for Chronic Conditions (a cura di), Parkinson’s Disease, London, Royal College of Physicians, 2006, 29–47. ISBN 1-86016-283-5
- ^ a b c d e Brooks DJ (April 2010). Imaging approaches to Parkinson disease. J. Nucl. Med. 51 (4): 596–609. DOI:10.2967/jnumed.108.059998.
- ^ Godau, J. (Apr 2012). Neuroimaging: current role in detecting pre-motor Parkinson’s disease.. Mov Disord 27 (5): 634-43. DOI:10.1002/mds.24976. PMID 22508281.
- ^ Kim, JS.. Transcranial sonography (TCS) in Parkinson’s disease (PD) and essential tremor (ET) in relation with putative premotor symptoms of PD.. Arch Gerontol Geriatr 54 (3): e436-9. DOI:10.1016/j.archger.2012.01.001. PMID 22277379.
- ^ Izawa Okawa, M. (Apr 2012). [Transcranial sonography findings in Parkinson’s disease].. Brain Nerve 64 (4): 413-22. PMID 22481514.
- ^ Sakalauskas, A. (Apr 2012). Automated segmentation of transcranial sonographic images in the diagnostics of Parkinson’s disease.. Ultrasonics. DOI:10.1016/j.ultras.2012.04.005. PMID 22578750.
- ^ Eidelberg, op. cit., pp. 3-8.
- ^ Eidelberg, op. cit., pp. 11-17.
- ^ Poewe W, Wenning G (November 2002). The differential diagnosis of Parkinson’s disease. Eur. J. Neurol. 9 (Suppl 3): 23–30. DOI:10.1046/j.1468-1331.9.s3.3.x.
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab ac ad ae Symptomatic pharmacological therapy in Parkinson’s disease in The National Collaborating Centre for Chronic Conditions (a cura di), Parkinson’s Disease, London, Royal College of Physicians, 2006, 59–100. ISBN 1-86016-283-5
- ^ a b Bronstein JM, Tagliati M, Alterman RL, et al. (February 2011). Deep brain stimulation for Parkinson disease: an expert consensus and review of key issues. Arch. Neurol. 68 (2). DOI:10.1001/archneurol.2010.260.
- ^ a b Palliative care in Parkinson’s disease in The National Collaborating Centre for Chronic Conditions (a cura di), Parkinson’s Disease, London, Royal College of Physicians, 2006, 147–51. ISBN 1-86016-283-5
- ^ Tolosa E, Katzenschlager R, Pharmacological management of Parkinson’s disease in Tolosa E, Jankovic JJ (a cura di), Parkinson’s disease and movement disorders, Hagerstwon, MD, Lippincott Williams & Wilkins, 2007, 110–45. ISBN 0-7817-7881-6
- ^ Goldenberg MM (October 2008). Medical management of Parkinson’s disease. P & T 33 (10): 590–606.
- ^ a b Non-motor features of Parkinson’s disease in The National Collaborating Centre for Chronic Conditions (a cura di), Parkinson’s Disease, London, Royal College of Physicians, 2006, 113–33. ISBN 1-86016-283-5
- ^ Hasnain M, Vieweg WV, Baron MS, Beatty-Brooks M, Fernandez A, Pandurangi AK (July 2009). Pharmacological management of psychosis in elderly patients with parkinsonism. Am. J. Med. 122 (7): 614–22. DOI:10.1016/j.amjmed.2009.01.025.
- ^ Gagne JJ, Power MC (Mar 2010). Anti-inflammatory drugs and risk of Parkinson disease: a meta-analysis. Neurology 74 (12): 995–1002. DOI:10.1212/WNL.0b013e3181d5a4a3.
- ^ a b c d Surgery for Parkinson’s disease in The National Collaborating Centre for Chronic Conditions (a cura di), Parkinson’s Disease, London, Royal College of Physicians, 2006, 101–11. ISBN 1-86016-283-5
- ^ Limousin, P. (Oct 1998). Electrical stimulation of the subthalamic nucleus in advanced Parkinson’s disease.. N Engl J Med 339 (16): 1105-11. DOI:10.1056/NEJM199810153391603. PMID 9770557.
- ^ Weaver, FM. (Jan 2009). Bilateral deep brain stimulation vs best medical therapy for patients with advanced Parkinson disease: a randomized controlled trial.. JAMA 301 (1): 63-73. DOI:10.1001/jama.2008.929. PMID 19126811.
- ^ Genever, RW. (May 2009). Deep brain stimulation for patients with advanced Parkinson disease.. JAMA 301 (19): 1985; author reply 1985-6. DOI:10.1001/jama.2009.647. PMID 19454631.
- ^ a b c d e Other key interventions in The National Collaborating Centre for Chronic Conditions (a cura di), Parkinson’s Disease, London, Royal College of Physicians, 2006, 135–46. ISBN 1-86016-283-5
- ^ a b Goodwin VA, Richards SH, Taylor RS, Taylor AH, Campbell JL (April 2008). The effectiveness of exercise interventions for people with Parkinson’s disease: a systematic review and meta-analysis. Mov. Disord. 23 (5): 631–40. DOI:10.1002/mds.21922.
- ^ Dereli EE, Yaliman A (April 2010). Comparison of the effects of a physiotherapist-supervised exercise programme and a self-supervised exercise programme on quality of life in patients with Parkinson’s disease. Clin Rehabil 24 (4): 352–62. DOI:10.1177/0269215509358933.
- ^ O’Sullivan & Schmitz, op. cit., pp. 873-876.
- ^ O’Sullivan & Schmitz, op. cit., p. 879.
- ^ O’Sullivan & Schmitz, op. cit., p. 877.
- ^ O’Sullivan & Schmitz, op. cit., p. 880.
- ^ Fox CM, Ramig LO, Ciucci MR, Sapir S, McFarland DH, Farley BG (November 2006). The science and practice of LSVT/LOUD: neural plasticity-principled approach to treating individuals with Parkinson disease and other neurological disorders. Semin. Speech. Lang. 27 (4): 283–99. DOI:10.1055/s-2006-955118.
- ^ Dixon L, Duncan D, Johnson P, et al. (2007). Occupational therapy for patients with Parkinson’s disease. Cochrane Database Syst. Rev. (3): CD002813. DOI:10.1002/14651858.CD002813.pub2.
- ^ Koch G (2010). rTMS effects on levodopa induced dyskinesias in Parkinson’s disease patients: searching for effective cortical targets. Restor. Neurol. Neurosci. 28 (4): 561–8. DOI:10.3233/RNN-2010-0556.
- ^ Platz T, Rothwell JC (2010). Brain stimulation and brain repair—rTMS: from animal experiment to clinical trials—what do we know?. Restor. Neurol. Neurosci. 28 (4): 387–98. DOI:10.3233/RNN-2010-0570.
- ^ Arias P, Vivas J, Grieve KL, Cudeiro J (September 2010). Controlled trial on the effect of 10 days low-frequency repetitive transcranial magnetic stimulation (rTMS) on motor signs in Parkinson’s disease. Mov. Disord. 25 (12): 1830–8. DOI:10.1002/mds.23055.
- ^ Suchowersky O, Gronseth G, Perlmutter J, Reich S, Zesiewicz T, Weiner WJ (April 2006). Practice Parameter: neuroprotective strategies and alternative therapies for Parkinson disease (an evidence-based review): report of the Quality Standards Subcommittee of the American Academy of Neurology. Neurology 66 (7): 976–82. DOI:10.1212/01.wnl.0000206363.57955.1b.
- ^ Lee MS, Lam P, Ernst E (December 2008). Effectiveness of tai chi for Parkinson’s disease: a critical review. Parkinsonism Relat. Disord. 14 (8): 589–94. DOI:10.1016/j.parkreldis.2008.02.003.
- ^ Lee MS, Ernst E (January 2009). Qigong for movement disorders: A systematic review. Mov. Disord. 24 (2): 301–3. DOI:10.1002/mds.22275.
- ^ Lee MS, Shin BC, Kong JC, Ernst E (August 2008). Effectiveness of acupuncture for Parkinson’s disease: a systematic review. Mov. Disord. 23 (11): 1505–15. DOI:10.1002/mds.21993.
- ^ Katzenschlager R, Evans A, Manson A, et al (2004). Mucuna pruriens in Parkinson’s disease: a double blind clinical and pharmacological study. J. Neurol. Neurosurg. Psychiatr. 75 (12): 1672–7. DOI:10.1136/jnnp.2003.028761.
- ^ Ladha SS, Walker R, Shill HA (May 2005). Case of neuroleptic malignant-like syndrome precipitated by abrupt fava bean discontinuance. Mov. Disord. 20 (5): 630–1. DOI:10.1002/mds.20380.
- ^ Raguthu L, Varanese S, Flancbaum L, Tayler E, Di Rocco A (October 2009). Fava beans and Parkinson’s disease: useful ‘natural supplement’ or useless risk?. Eur. J. Neurol. 16 (10): e171. DOI:10.1111/j.1468-1331.2009.02766.x.
- ^ a b Hoehn, MM. (May 1967). Parkinsonism: onset, progression and mortality.. Neurology 17 (5): 427-42. PMID 6067254.
- ^ a b c d e f g h i j k l Poewe W (December 2006). The natural history of Parkinson’s disease. J. Neurol. 253 (Suppl 7): VII2–6. DOI:10.1007/s00415-006-7002-7.
- ^ Goetz, CG. (Sep 2004). Movement Disorder Society Task Force report on the Hoehn and Yahr staging scale: status and recommendations.. Mov Disord 19 (9): 1020-8. DOI:10.1002/mds.20213. PMID 15372591.
- ^ a b c d e Findley LJ (September 2007). The economic impact of Parkinson’s disease. Parkinsonism Relat. Disord. 13 (Suppl): S8–S12. DOI:10.1016/j.parkreldis.2007.06.003.
- ^ a b Parkinson’s – ‘the shaking palsy’. GlaxoSmithKline, 2009-04-01
- ^ National Parkinson Foundation – Mission. URL consultato in data 2011-03-28.
- ^ (1960-01-18) Education: Joy in Giving. Time. URL consultato in data 2011-04-02.
- ^ About PDF. Parkinson’s Disease Foundation. URL consultato in data 2011-10-02.
- ^ American Parkinson Disease Association: Home. American Parkinson Disease Association, Inc. URL consultato in data 2010-08-09.
- ^ About EPDA. European Parkinson’s Disease Association, 2010. URL consultato in data 2010-08-09.
- ^ a b Davis P. Michael J. Fox. The TIME 100, Time, 2007-05-03. URL consultato in data 2011-04-02.
- ^ a b Brockes E. ‘It’s the gift that keeps on taking’. The Guardian, 2009-04-11. URL consultato in data 2010-10-25.
- ^ Michael J. Fox to be made honorary doctor at Karolinska Institutet, Karolinska Institutet, 2010-03-05. URL consultato in data 2011-04-02.
- ^ Roelofs T. Tour de France bicyclist Davis Phinney talks about life with Parkinson’s Disease, The Grand Rapids Press, 2010-05-10. URL consultato in data 2010-10-25.
- ^ Who We Are. Davis Phinney Foundation. URL consultato in data 2012-01-18.
- ^ Emanuel, W. Davis Phinney foundation launches exercise-focused tools to help people live well with Parkinson’s. Davis Phinney foundation, 2010-10-19. URL consultato in data 2011-04-02.
- ^ Brey RL (April 2006). Muhammad Ali’s Message: Keep Moving Forward (American Academy of Neurology) 2 (2). URL consultato in data 2011-04-02.
- ^ a b Matthews W (April 2006). Ali’s Fighting Spirit (American Academy of Neurology) 2 (2): 10–23. URL consultato in data 2011-04-02.
- ^ Tauber P. Ali: Still Magic. New York Times, 1988-07-17. URL consultato in data 2011-04-02.
- ^ a b Dimond PF. No New Parkinson Disease Drug Expected Anytime Soon in GEN news highlights. GEN-Genetic Engineering & Biotechnology News, 2010-08-16
- ^ Langston JW, Ballard P, Tetrud JW, Irwin I (February 1983). Chronic Parkinsonism in humans due to a product of meperidine-analog synthesis. Science 219 (4587): 979–80. DOI:10.1126/science.6823561.
- ^ Cicchetti F, Drouin-Ouellet J, Gross RE (September 2009). Environmental toxins and Parkinson’s disease: what have we learned from pesticide-induced animal models?. Trends Pharmacol. Sci. 30 (9): 475–83. DOI:10.1016/j.tips.2009.06.005.
- ^ Harvey BK, Wang Y, Hoffer BJ (2008). Transgenic rodent models of Parkinson’s disease. Acta Neurochir. Suppl. 101: 89–92. DOI:10.1007/978-3-211-78205-7_15.
- ^ Feng, LR, Maguire-Zeiss KA (2010). Gene Therapy in Parkinson’s Disease: Rationale and Current Status. CNS Drugs 24 (3): 177–92. DOI:10.2165/11533740-000000000-00000.
- ^ Lewitt PA, Rezai AR, Leehey MA, et al. (April 2011). AAV2-GAD gene therapy for advanced Parkinson’s disease: a double-blind, sham-surgery controlled, randomised trial. Lancet Neurol 10 (4): 309–19. DOI:10.1016/S1474-4422(11)70039-4.
- ^ Kuan, WL. (Dec 2011). A novel neuroprotective therapy for Parkinson’s disease using a viral noncoding RNA that protects mitochondrial Complex I activity.. J Exp Med. DOI:10.1084/jem.20111126. PMID 22184634.
- ^ Ebadi, M. (Feb 2002). Neuroprotective actions of selegiline.. J Neurosci Res 67 (3): 285-9. PMID 11813232.
- ^ World’s first Parkinson’s vaccine is trialled. New Scientist, 2012-06-07
- ^ Redmond DE (October 2002). Cellular replacement therapy for Parkinson’s disease—where we are today?. The Neuroscientist 8 (5): 457–88. DOI:10.1177/107385802237703.
- ^ Nuovo ruolo di NURR1 e malattia di Parkinson. URL consultato in data 20 ottobre 2012.
- ^ Stem Cell Research Aims to Tackle Parkinson’s Disease. URL consultato in data 2010-04-16.
- ^ Pande lab. About Folding@home in Folding@home. Stanford University, August 2, 2012 (archiviato dall’url originale)
Bibliografia
- Fazio C, Loeb C, Favale E, Neurologia, Società Editrice Universo, 2003. ISBN 8887753733
- Luigi Ravizza, Invecchiamento cerebrale e demenze, Elsevier srl, 2004. ISBN 9788821427169
- Diego De Leo, Manuale di Psichiatria dell’Anziano, PICCIN, 1994. ISBN 9788829911851
- (EN) Douglas M. Anderson; A. Elliot Michelle, Mosby’s medical, nursing, & Allied Health Dictionary sesta edizione, New York, Piccin, 2004. ISBN 88-299-1716-8
- (EN) Susan B. O’Sullivan, Thomas J. Schmitz, Parkinson’s Disease in Physical Rehabilitation, 5th, Philadephia, F.A. Davis, 2007. ISBN 978-0803612471
- (EN) David Eidelberg, Imaging in Parkinson’s Disease, Oxford University Press, 2011. ISBN 9780195393484
- (EN) Dickson DV, Neuropathology of movement disorders in Parkinson’s disease and movement disorders, Hagerstown, MD, 2007. ISBN 0-7817-7881-6