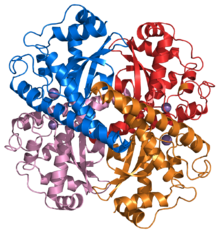
Superossido Dismutasi
Senza ossigeno non potremmo vivere. Le nostre cellule usano l’ossigeno come accettore finale di elettroni nella respirazione, in questo modo riescono a ricavare molta più energia dal cibo di quanto farebbero in condizioni anaerobiche.
L’ossigeno però è anche un composto pericoloso. Forme reattive dell’ossigeno come il radicale superossido (ossigeno con un elettrone in più) possono sfuggire agli enzimi della respirazione cellulare e provocare disastri nelle cellule. Il superossido può anche causare mutazioni nel DNA o attaccare gli enzimi che sintetizzano amminoacidi o altre molecole essenziali. Questo non è un pericolo trascurabile: una ricerca ha dimostrato che circa ogni 10 mila elettroni trasferiti lungo la catena respiratoria nelle cellule di Escherichia coli, tre elettroni finiscono per produrre superossido invece di seguire il loro normale percorso fino all’enzima che li trasferisce all’ossigeno per produrre acqua. Per combattere questo pericolo la maggior parte delle cellule produce l’enzima Superossido Dismutasi (SOD) che trasforma il superossido in molecole meno pericolose (ossigeno e acqua ossigenata).
Dismutazione
Come si intuisce dal nome, l’enzima SOD (mostrato qui dal file PDB 2sod) dismuta il superossido. La dismutazione è un particolare tipo di reazione nella quale avvengono contemporaneamente due reazioni opposte, un’ossidazione e una riduzione, su due molecole uguali. L’enzima SOD prende due radicali superossido, strappa via l’elettrone in più dal primo e lo trasferisce al secondo. In questo modo una delle due molecole si ritrova con un elettrone in meno e quindi diventa ossigeno molecolare O2, l’altra si ritrova con un elettrone in più e, dopo aver legato due ioni H+, diventa acqua ossigenata H2O2.
Poichè anche l’acqua ossigenata è un composto pericoloso, la cellula cerca di distruggerla nel più breve tempo possibile.usando l’enzima Catalasi (Molecola del Mese del settembre 2004).
L’enzima SOD in Medicina
L’enzima Superossido Dismutasi SOD ha recentemente guadagnato notorietà perchè si è scoperto che è implicato nella Sclerosi Laterale Amiotrofica. Questa è una grave malattia degenerativa che porta alla morte selettiva dei motoneuroni nel sistema nervoso centrale e nel midollo spinale, e porta ad una paralisi progressiva e irreversibile nel giro di pochi anni.
La maggior parte dei casi di SLA si verificano in età adulta e la sua causa era, fino a poco tempo fa, sconosciuta. Circa il dieci per cento dei casi di SLA sono ereditari, provocati da mutazioni genetiche che vengono trasmesse ai figli. Una ricerca ha da poco dimostrato che una di queste mutazioni si trova nel gene che codifica per l’enzima SOD. Gli scienziati stanno ora studiando il ruolo dell’enzima SOD in questa malattia sperando di scoprire qualcosa che porti a nuovi trattamenti e a cure più efficaci.
Metalli Pesanti
Quasi tutti gli organismi possiedono una qualche forma di Superossido Dismutasi (SOD), così esistono varianti di questo enzima con strutture anche molto diverse tra loro. Tutti questi enzimi però hanno una caratteristica comune: usano ioni di metalli pesanti per realizzare la reazione di trasferimento degli elettroni.
Le nostre cellule producono tre tipi di SOD.
Un primo tipo, che contiene ioni rame e zinco (mostrato qui dal file PDB 1sos), si muove intorno alla cellula per catturare eventuali molecole di superossido formate prima che l’ossigeno entri nella cellula.
Un secondo tipo di SOD, simile al primo e quindi anche questo con rame e zinco, possiede una coda appiccicosa che lo fissa alle strutture all’esterno della cellula.
Un terzo tipo di SOD, che contiene ioni manganese (mostrato qui dal file PDB 1msd), viene prodotto nei mitocondri, il punto più a rischio per la sintesi accidentale di superossido, infatti qui è localizzata la catena respiratoria e gli elettroni vengono trasferiti all’ossigeno per ridurlo ad acqua.
I batteri costruiscono una varietà di enzimi SOD come i due mostrati qui, uno contiene ioni ferro (file PDB 3sdp) e l’altro, cosa insolita, contiene ioni nichel (file PDB 1q0d).
Esplorando la Struttura
L’enzima Cu/Zn Superossido Dismutasi che contiene ioni rame e zinco (file PDB 2sod) è estremamente efficiente.
Alcuni ricercatori hanno calcolato che una collisione su dieci tra il radicale superossido e l’enzima porta ad una reazione. Questo è molto più di quanto ci si aspettasse perchè il sito attivo dell’enzima occupa solo una piccola parte della superficie della proteina e quindi si potrebbe pensare che la maggior parte delle collisioni con il superossido avvengano in qualche altro punto della superficie e non nel sito attivo. La forma e le caratteristiche del sito attivo, però, ci possono dare una spiegazione di tanta efficienza.
Il sito attivo ha una forma ad imbuto e gli ioni rame e zinco (mostrati in verde) sono posti sul fondo dell’imbuto. La forte carica positiva di questi ioni metallici insieme con la carica positiva di due amminoacidi vicini (una lisina e un’arginina colorate in blu) può costringere il radicale superossido, negativo (mostrato in rosso), ad entrare nell’imbuto.
Queste figure sono state create con RasMol (Chime) (vedi Chimica al Computer). Anche voi potete creare immagini simili seguendo questa procedura: cliccate sui codici di accesso PDB qui sopra per scaricare il file compresso (zip) della proteina, decomprimetelo e poi lanciatelo con Internet Explorer. Se avete installato Chime, potrete scegliere nel menù Display le opzioni di visualizzazione che desiderate.
Fonte articolo
http://www.pianetachimica.it/mol_mese/mol_mese_2007/10_Superossido/Superossido_1.htm