Con il termine “epatiti croniche” sono indicate numerose affezioni di varia estensione, evolutività e gravità, a diversa eziologia, che presentano in comune l’interessamento del fegato da parte di un processo infiammatorio cronico per lo più a partenza dagli spazi portali, e associato a compromissione parenchimale con necrosi epatocellulare. Molte di queste forme hanno una tendenza spontanea all’automantenimento e possono pertanto evolvere progressivamente verso la cirrosi, ovvero stabilizzarsi per lunghissimi periodi o anche indefinitivamente. In altre condizioni, qualora l’agente eziologico venga rimosso, il danno epatico può invece andare incontro a regressione, magari con una modesta fibrosi residua.
CLASSIFICAZIONE
Una prima classificazione delle epatiti croniche fu proposta circa trenta anni fa, quando la maggior parte degli agenti eziologici attualmente noti era allora sconosciuta, cosicché una patogenesi su base immunologica fu prospettata per molte di esse. Negli anni a seguire, la scoperta dei diversi virus epatitici e le nuove conoscenze sulla patogenesi delle epatiti croniche hanno portato al progressivo ampliamento dei criteri classificativi preesistenti, pur mantenendo la grande enfasi attribuita agli aspetti istologici: vennero così coniati i termini di epatite cronica persistente, lobulare e attiva, intese come forme di epatopatia cronica a carattere evolutivo, a eziologia quasi sempre virale, ed il cui utilizzo nella pratica clinica consentiva (e consente tuttora) un approccio terapeutico ben codificato.
Secondo la vecchia nomenclatura, nell’epatite cronica persistente la flogosi cronica interessa gli spazi portali, conservando sostanzialmente l’integrità della struttura lobulare, senza fibrosi o necrosi della lamina limitante (ovvero della schiera di epatociti che delimita lo spazio portale stesso), e con una modesta sofferenza parenchimale. Questi due aspetti vennero considerati essenziali per la diagnosi differenziale con l’epatite cronica attiva, o aggressiva (vedi oltre), non essendo la distinzione tra le due forme sempre agevole sul piano clinico: infatti, l’assenza o la minor entità della compromissione delle condizioni generali e delle alterazioni bioumorali, in genere limitate all’aumento delle transaminasi, non sempre si correla con l’attività della malattia.
La cosiddetta epatite cronica lobulare, che tra l’altro rappresentava un’entità nosologica non accettata da tutti gli autori, risulta del tutto sovrapponibile all’epatite cronica persistente per le caratteristiche cliniche, il quadro bioumorale, l’eziopatogenesi e la prognosi. Da un punto di vista istologico l’epatite cronica lobulare veniva caratterizzata da un infiltrato flogistico localizzato all’interno del lobulo epatico, costituito da elementi cellulari prevalentemente linfocitari, con associati più evidenti fenomeni degenerativi e necrotici a carico degli epatociti. Analogamente alla cosiddetta epatite cronica persistente, anche in questa forma la lamina limitante è rispettata, come pure l’architettura lobulare, e la fibrosi è assente.
Infine, l’epatite cronica attiva rappresenta un’entità nosologica nella quale ben evidenti sono gli aspetti evolutivi, sia sul piano bioumorale sia soprattutto su quello istologico, caratterizzato da un evidente infiltrato flogistico e da una fibrosi più o meno estesa, che interessa gli spazi portali ed invade più o meno estesamente il parenchima circostante oltre la lamina limitante, a configurare la cosiddetta peripheral piecemeal necrosis. Gliepatociti presentano infine fenomeni di necrosi parcellare cui si associano tipici fenomeni regressivi.
Questa suddivisione in tre forme distinte ha dato tuttavia luogo a numerose critiche, dovute principalmente al fatto che la distinzione non sempre poteva essere basata su criteri diagnostici univoci, mancando di qualunque criterio semiquantitativo di graduazione e di stadiazione; inoltre le caratteristiche epidemiologiche e cliniche sono sotto molti aspetti sovrapponibili, se si eccettua che nell’epatite cronica persistente ed in quella lobulare i sintomi sono generalmente più sfumati o talvolta assenti, e che l’esordio clinico e sintomatologico è di solito anticipato, interessando soprattutto soggetti appartenenti alla terza e quarta decade di vita. In aggiunta, è importante sottolineare che l’aspetto istologico di un’epatite cronica attiva in stabilizzazione o in remissione (come ad esempio in seguito a trattamento interferonico), può essere in pratica indistinguibile da una forma persistente, e che vi sono forme al limite fra persistente (o lobulare) e attiva (definite come borderline), nelle quali non è possibile stabilire con esattezza l’atteggiamento terapeutico da seguire. Infine, per quanto il decorso di un’epatite cronica persistente o lobulare risultasse sostanzialmente benigno, almeno nelle fasi iniziali, in una significativa percentuale di casi (oscillante tra il 10 ed il 20%) è stata poi documentata l’evoluzione in una forma attiva e successivamente anche verso la cirrosi.
Negli anni più recenti è stata pertanto proposta una definizione di epatite cronica che prende in considerazione anche aspetti clinici e microbiologici, in associazione a tutte le nozioni di tipo istopatologico già acquisite da tempo, e che considera come criterio di scelta iniziale quello eziologico, per le diverse caratteristiche di decorso, di prognosi e di terapia che ogni diversa forma di epatite cronica possiede.
Nel contesto di ogni distinta forma, alle alterazioni istopatologiche, talora patognomoniche, può essere attribuito un punteggio in termini di graduazione (grading) e stadiazione (staging), al fine di ottenere una standardizzazione di tipo semiquantitativo. In tal modo, viene abbandonata la tendenza a distinguere le forme di epatite cronica in persistente, lobulare e attiva, utilizzata in passato, venendo a considerare queste forme come un’unica malattia, a differente severità.
Numerose sono le epatopatie che possono presentarsi con una compromissione prevalente degli spazi portali e che per alcune caratteristiche istologiche e cliniche somigliano ad un’epatite cronica virale, e che pertanto vanno considerate ed escluse nella diagnosi differenziale. Tra queste, le forme più frequenti sono l’epatite autoimmune, la cirrosi biliare primitiva e la colangite sclerosante primaria, dove le lesioni a carico degli epatociti sono tuttavia secondarie all’estensione della flogosi che origina dai dotti biliari; viceversa, nel morbo di Wilson e nella forma da deficit di (a1‑antitripsina, dovute a patologie determinate geneticamente e spesso con evidenti manifestazioni sistemiche, il coinvolgimento parenchimale è prevalente, almeno inizialmente, e solo successivamente coinvolgerà gli spazi portali.
L’epatite cronica a eziologia virale viene pertanto oggi definita come un processo necro‑infiammatorio del fegato a diversa eziologia, che si mantiene per oltre 6 mesi e si caratterizzata istologicamente per la presenza di un infiltrato flogistico degli spazi portali e di sofferenza epatocellulare, con aree di necrosi più o meno estese e localizzate alla periferia del lobulo, ed erosione della lamina limitante. Nella stragrande maggioranza dei casi, è inoltre osservabile una chiara tendenza all’evoluzione verso la fibrosi o la cirrosi epatica.
Come già accennato, la più recente classificazione delle diverse forme di epatite cronica segue innanzitutto un criterio eziopatogenetico, e può essere così rappresentata:
Anche alcuni farmaci, specie se assunti per periodi protratti, sono in grado di causare forme di epatite cronica aventi caratteristiche cliniche ed istologiche simili alle forme virali od autoimmuni, ma queste forme solo raramente assumono caratteristiche evolutive. Inoltre, questi agenti terapeutici sono stati a volte ritenuti gli agenti causali di un’epatite cronica autoimmune, potendo indurre, durante il trattamento, la comparsa di autoanticorpi anti‑nudeo (ANA), o anti‑microsomi del fegato e del rene (LKM1) a basso titolo. Tra i farmaci ritenuti più frequentemente implicati sono da citare l’ossifenisatina, impiegata soprattutto in passato come lassativo, ed in certi casi l’alotano o la metildopa, anche se virtualmente ogni sostanza è in grado di provocare, in soggetti predisposti, un processo epatitico cronico, la cui attività tuttavia si riduce progressivamente con la sospensione dell’assunzione del farmaco, lasciando solo modesti reliquati. Una considerazione a parte merita la clorpromazina, che è capace di indurre nel 2 % dei casi una forma epatitica di tipo colestatico, spesso evolvente in cirrosi biliare secondaria.
Per epatiti croniche criptogenetiche si intendono tutte quelle forme nelle quali ogni possibile movente patogenetico (infettivo, metabolico, autoimmunologico, farmacologico o tossicologico) sia stato accuratamente escluso; questi casi, che in certe casistiche raggiungono anche il 20% circa di tutte le epatiti croniche, possono essere almeno in parte dovuti ad infezioni determinate da virus epatotropi non ancora identificati.
In questa sede verrà riservata particolare attenzione alle epatiti croniche ad eziologia virale ed all’epatite cronica autoimmune, che oltre a rappresentare le forme di più frequente riscontro, sono anche quelle ormai più compiutamente caratterizzate. Verranno in seguito considerate quelle forme che un tempo furono definite, talora in maniera non sempre appropriata, come epatiti croniche non evolutive, e che comprendono l’epatite cronica alcolica, l’epatite reattiva aspecifica, le epatiti croniche specifiche, nonché le più comuni epatiti batteriche e parassitarie.
EPATITI CRONICHE VIRALI
Negli ultimi decenni, ben sei diversi virus epatitici sono stati identificati e spesso in gran parte caratterizzati (A, B, C, D, o virus delta, E e G). L’infezione da virus A ed E viene trasmessa per via oro‑fecale e virtualmente non conduce mai alla cronicizzazione, mentre poco chiari sono ancora i dati riguardanti le caratteristiche del virus G e le potenzialità evolutive delle forme acute da esso sostenute. D’altra parte, i virus B, delta e C rappresentano invece gli agenti eziologici principali delle forme di epatite cronica ed anche di cirrosi, e verranno pertanto considerati più estesamente in questa sede.
Resta comunque tuttora valida la dizione di epatite cronica non A‑E per quelle forme in cui l’eziologia virale è più probabile sulla base delle caratteristiche epidemiologiche (per esempio post‑trasfusionalí), cliniche, bioumorali ed istologiche; in questo gruppo potrebbe ancora essere opportuno considerare le forme dovute con alta probabilità al virus G dell’epatite, anch’esso trasmissibile a soggetti sottoposti a terapia emodialitica o trasfusionale; l’HGV rappresenta l’agente eziologico identificato nel 6‑14% delle epatopatie ritenute un tempo criptogenetiche, ma aventi caratteristiche cliniche sovrapponibili a quelle delle altre forme ad eziologia sicuramente virale, nell’attesa che test diagnostici specifici per questo agente ne consentano una più precisa caratterizzazione, soprattutto per quanto riguarda la potenzialità di dare origine a forme croniche, che resta ancora da definire compiutamente.
E’ ormai chiaro che nella patogenesi della cronicizzazione delle epatiti virali, il danno epatico rappresenta la risultante dell’attivazione e del mantenimento di una risposta immunitaria citotossica diretta contro antigeni autologhi o eterologhi (in questo caso virali) esposti sulla membrana degli epatociti. In linea generale, in molti soggetti infettati da virus epatitici l’espressione di antigeni virali sulla membrana dell’epatocita infettato, in associazione con antigeni di istocompatibilità del complesso HLA, porta al loro riconoscimento da parte del sistema immune, sia umorale che cellulare (soprattutto linfociti T citotossici), la cui attivazione avrebbe lo scopo di eliminare definitivamente le cellule infettate e quindi l’infezione virale. Virus epatitici quali l’HBV e FHCV possiedono invece alcune proprietà biologiche che consentono loro, in determinate circostanze ed in soggetti predisposti, di eludere almeno in parte il sistema immunitario impedendo l’eradicazione completa dell’infezione.
Ad esempio, in corso di infezione da HBV, la risposta immunitaria cellulo‑mediata viene diretta contro gli epitopi delle proteine del nucleocapside virale, dell’envelope e della DNA polimerasi, e molto spesso risulta in grado di interrompere e poi di eradicare la replicazione virale limitando progressivamente il processo infiammatorio intraepatico fino alla guarigione definitiva, come avviene in tutti i casi di epatite acuta. Questi fenomeni si realizzano anche in virtù della capacità dei linfociti T citotossici attivati di sintetizzare numerose citochine (soprattutto IFN‑y e TNF‑(x) capaci di inibire la replicazione del virus senza peraltro danneggiare la cellula ospite. Tuttavia, nei casi in cui il sistema immunitario non sia in grado di eliminare completamente il virus dagli epatociti, il persistere dell’affivazione linfocitaria potrà causare un danno protratto a carico del fegato.
Le forme sostenute dal virus B dell’epatite sono attualmente molto meno frequenti che in passato, anche per la progressiva eradicazione dell’endemia in certe aree geografiche, resa possibile dall’avvento della vaccinazione. La distribuzione dell’infezione da HBV varia considerevolmente da regione a regione, essendovi nel mondo aree geografiche ad elevata prevalenza come il Sud Est Asiatico, la Cina ed alcuni paesi africani, dove oltre l’8% della popolazione risulta portatore cronico del virus, in virtù dell’alta incidenza di trasmissione verticale. D’altra parte, in aree considerate a basso grado di endemicità, quali il Nordamerica, l’Europa occidentale e l’Australia, la trasmissione è prevalentemente di tipo orizzontale, e nei giovani adulti. Attualmente, si calcola che negli Stati Uniti oltre un milione di persone siano portatrici croniche del virus, mentre in Italia la prevalenza è di circa 200.000, e la trasmissione dell’infezione avviene prevalentemente per contagio di tipo sessuale o tramite scambio di siringhe infette; più raramente, la trasmissione dell’infezione da HBV avviene in seguito a procedure medico‑ chirurgiche, emotrasfusioni o emodialisi.
L’HBV è in grado di eludere la sorveglianza immunitaria sia umorale che cellulare e quindi di mantenere l’infezione all’interno degli epatociti grazie alla sua variabilità genetica, che consente la selezione di ceppi mutanti. Infatti, la mutazione anche di un solo aminoacido della proteina di superficie dell’HBsAg consente di sfuggire all’effetto neutralizzante degli anticorpi anti‑HBs diretti contro questo antigene, che sono normalmente in grado di bloccare i siti recettoriali di membrana che consentono al virus di infettare nuove cellule. Inoltre, sono state descritte mutazioni a livello di alcuni epitopi (ma non di tutti) abitualmente riconosciuti dai linfociti T citotossici: in queste condizioni, l’evasione solo parziale alla risposta immune ne comporta un’attivazione praticamente costante, che mantiene cronicamente 9 danno epatico. Infine, in virtù di particolari mutazioni, certi ceppi virali sono in grado di bloccare la sintesi delle proteine che rappresentano il bersaglio del riconoscimento anticorpale: l’esempio più eclatante è la mutazione che si realizza a livello della regione pre‑core dell’HBV con mancata produzione e liberazione in circolo dell’HBeAg, uno dei principali bersagli dei linfociti T.
Il virus delta dell’epatite (o HDV) è in grado di provocare un processo epatitico solo se l’ospite è infettato anche dalHBV, che svolge funzioni di helper consentendo all’HDV la penetrazione, l’assemblaggio ed il rilascio in circolo degli elementi virali completi. L’incidenza dell’infezione da HDV in soggetti HbsAg positivi è attualmente stimata intorno al 2% circa, ma sale al 9% nei tossicodipendenti. Tale infezione può avvenire sia contemporaneamente a quella da HBV (coinfezione), oppure sovrapporsi ad un’infezione cronica preesistente (superinfezione), che consentirebbe la diffusione intraepatica e la cronicizzazione anche dell’infezione da HDV. La gravità con cui un’infezione da HDV si manifesta dipende dalle caratteristiche virologiche presenti al momento del contagio.. Infatti, qualora la malattia da HBV sia in fase di elevata replicazione virale, la superinfezione rappresenta un’ulteriore spinta evolutiva, mentre l’assenza defl’HBV‑DNA, con quindi esclusiva presenza di marcatori di danno HDV‑correlato, comporta un decorso prolungato e paucisintomatico, con evoluzione cirrogena tardiva.
L’HCV è senza dubbio l’agente virale più frequentemente causa di epatite cronica: dati recenti indicano che negli Stati Uniti circa 4 milioni di persone sono portatrici dell’infezione da HCV, con 150.000 nuovi casi ogni anno, mentre in Italia la prevalenza stimata è di oltre 2 milioni di persone portatrici di anticorpi anti‑HCV. Inoltre, si calcola che circa 12.000 decessi ogni anno siano da imputare alle complicanze (cirrosi, epatocarcinoma) di un’epatite cronica da HCV. Dopo l’episodio acuto, che in meno del 25% dei casi è clinicamente ben evidente, oltre l’80% dei soggetti mantiene l’infezione, che con elevata frequenza (superiore al 50%) va incontro a cronicizzazione.
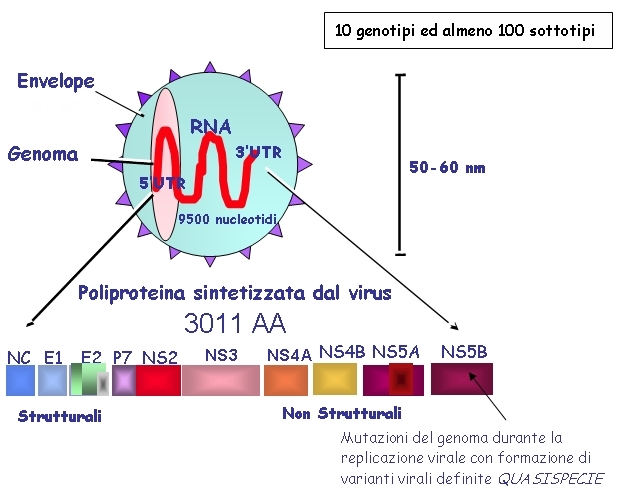
Numerose evidenze sperimentali attualmente ritengono che in corso di epatite da HCV i meccanismi di cronicizzazione (un tempo imputati al solo effetto citopatico diretto del virus) siano per molti aspetti simili a quanto già ricordato a proposito dell’HBV. Sebbene i meccanismi grazie ai quali l’infezione da HCV persiste nonostante un’appropriata competenza immunologica dell’ospite siano stati chiariti solo in parte, è ormai certo che la persistenza del virus e quindi la frequentissima cronicizzazione siano da imputare all’estrema variabilità del genoma dell’HCV: ciò ne ha comportato la denominazione di “quasispecie”, ad indicare simili (seppur eterogenei) e numerosi ceppi virali distinti, ma coesistenti nello stesso individuo, che consentono al virus di eludere abbastanza agevolmente la risposta immunitaria dell’ospite, sia umorale che cellulo‑mediata. All’interno del genoma dell’HCV è stata infatti individuata una regione ipervariabile (HVR1) localizzata nella regione E2/NS1 codificante per quelle sequenze aminoacidiche che rappresenterebbero uno dei possibili bersagli della risposta anticorpale. L’elevata variabilità di dette sequenze fa sì che queste siano costantemente neutralizzate da anticorpi specifici, ma con successiva nuova produzione di varianti diverse, che sfuggono al controllo da parte di anticorpi neutralizzanti. Inoltre, da studi più recenti appare anche che, con meccanismi analoghi, e dovuti alla presenza di numerose altre regioni ipervariabili localizzate all’interno del genoma virale (core, E1, NS3, NS4B, NS5B), il virus sia in grado anche di eludere la sorveglianza immunitaria cellulomediata, esercitata principalmente da linfociti‑T citotossici.
Infine, PHCV possiede la capacità di replicarsi anche in sedi extraepatiche, soprattutto in cellule del sistema immune (monociti e linfociti B e T): ciò potrebbe alterare in qualche modo la reattività a stimoli antigenici da parte di questi elementi che, oltre a contribuire al perdurare ed al cronicizzare dell’infezione, potrebbe spiegare la patogenesi di alcune epatiti croniche autoimmuni ed anche di malattie a localizzazione extraepatica come la crioglobulinemia mista, i linforni non‑Hodgkin B e, secondo certi autori, anche alcune gammopatie monoclonali.
In alcuni soggetti con infezione cronica da HBV o da FICV, l’aggressione da parte dei linfociti T contro gli epatociti è rivolta non solo contro antigeni di origine virale, ma anche verso determinanti antigenici autologhi. Questa attivazione autoimmune sarebbe favorita da una relativa carenza di linfociti T suppressor (0KT8+) rispetto a quelli citotossici (0KT4+), che rappresentano i principali effettori della risposta immunitaria.
Altri fattori sono da considerare come concause nella patogenesi della cronicizzazione, quali alterazioni del fegato preesistenti o compresenti all’infezione (danno da farmaci o da alcol ecc.), che costituiscono un elemento di danno aggiuntivo.
Da sottolineare infine il fatto che la coinfezione HBV‑HCV è un fenomeno abbastanza raro, mentre molti soggetti, specie tossicodipendenti, possono presentare simultaneamente anticorpi anti‑HBc ed anti‑HCV, con tutti i segni clinici, umorali ed istologici di un’epatite cronica da virus C.
Il quadro clinico dell’epatite cronica ad eziologia virale è assai variabile, e soprattutto nelle forme da HCV è caratteristica l’alternanza di periodi di relativa quiescenza con fasi di riacutizzazione, non solo umorale (Fig.01), ma anche sintomatologica: la stragrande maggioranza dei pazienti presenta una malattia paucisintomatica o addirittura del tutto asintomatica: i sintomi, quando presenti, sono del tutto aspecifici e di intensità correlabile al grado di compromissione della funzionalità epatica; questi comprendono astenia e facile affaticabilità, anoressia, dimagrimento, vaghi disturbi dispeptici, raramente subittero e prurito, talvolta febbre. Come già accennato, in numerosi casi la malattia decorre per lungo tempo (anche 20‑40 anni) in maniera del tutto asintomatica e l’ipertransaminasemia in questi casi rappresenta un reperto occasionale, in occasione di esami biournorali eseguiti per altre cause. Raramente invece la diagnosi di epatite cronica viene posta durante il follow‑up di una epatite acuta, in quanto in oltre l’80% dei casi l’infezione acuta decorre in maniera anitterica ed asintornatica, senza segni clinici evidenti.
L’esame obiettivo evidenzia in genere un’epatomegalia, con un certo aumento di consistenza dell’organo, la cui superficie si mantiene peraltro liscia ed il margine smusso. La milza può anch’essa essere aumentata di dimensioni, ma una splenomegalia ben evidente è in genere l’espressione di forme già avanzate, e spesso progredite fino alla cirrosi. Analogamente, gli altri segni di epatopatia cronica rilevabili all’esame fisico del paziente (spider nevi, eritema palmare), sono generalmente assenti.
Come spesso accade per molte forme di epatopatia, i disturbi soggettivi lamentati dal paziente possono essere assai sfumati, per cui essa viene inizialmente sospettata in seguito al riscontro di alterazioni bioumorali in corso di esami eseguiti per altre cause, o più raramente in seguito alla dimostrazione della persistenza delle alterazioni a distanza di 6‑12 mesi da un episodio di epatite virale acuta. La diagnosi o il sospetto di un’epatopatia cronica sono basati sul corteo sintomatologico sopradescritto e sul persistente riscontro di un innalzamento delle transaminasi, variabile da paziente a paziente, e di durata superiore a 6 mesi, che solo nelle forme autoimmuni o nelle fasi di riacutizzazione delle forme da HCV raggiunge valori elevati (anche 10 volte la norma).
E’ assai arduo poter quantificare l’entità del danno epatico esistente sulla base della sola alterazione delle transaminasi, in quanto non esiste una correlazione lineare tra i livelli plasmatici raggiunti da AST e ALT ed il quadro istopatologico; analogamente, il pattern delle transaminasi non fornisce particolari indicazioni sulla diversa eziologia delle varie forme (nell’epatopatia alcolica può essere di ausilio il calcolo dell’indice di De Ritis, ovvero del rapporto AST/ALT, che è spesso maggiore di 2). Nelle forme da HCV, ad esempio, in molti pazienti le transaminasi possono essere normali o solo modicamente alterate, pur in presenza di un danno istologico evidente.
Gli altri indici di danno epatocellulare (LDH, OCT, etc.), risultano anch’essi lievemente alterati. Gli indici di colestasi sono invece per lo più normali o solo modicamente aumentati, e quindi poco attendibili ai fini della diagnosi: lay‑GT, infatti, rappresenta un test sensibile, ma poco specifico, di danno epatico, in quanto può essere misurata in concentrazioni plasmatiche aumentate anche in corso di danno epatico secondario ad alterazioni del metabolismo glucidico e lipidico (steatosi) o per l’azione dell’alcol o di numerosi farmaci (primi fra tutti i barbiturici e gli antiepilettici in genere). Analogamente, la fosfatasi alcalina può aumentare in modo consistente sia nelle forme virali con componente colestatica (Fig.02), sia nelle epatopatie colestatiche propriamente dette, sia in presenza di lesioni espansive, quali tumori, granulomi od ascessi, o per l’interessamento epatico in corso di malattie linfoproliferative o di amiloidosi. Infine, la bilirubinemia è il più delle volte normale o modicamente alterata, con aumento sia della quota libera che di quella coniugata, ed anche la colalemia, sia a digiuno che post‑prandiale, presenta in genere un moderato incremento.
Le y‑globuline (prevalententemente le IgG nelle forme virali e le IgA nelle forme alcoliche) aumentano in maniera variabile e poco prevedibile nei diversi pazienti; è comunque caratteristico un aumento marcato e precoce in corso di epatite autoímmune, dove precoce è anche la riduzione degli indici di funzionalità parenchimale (albuminemia, attività protrombinica e pseudocolinesterasi), che invece restano a lungo conservati nelle altre forme.
Con il progredire di un’epatite cronica verso la cirrosi, alle tipiche alterazioni istopatologiche fa riscontro un peggioramento del quadro bioumorale, soprattutto degli indici di funzionalità parenchimale protidosintetica, ed un decremento del numero di piastrine.
Infine, l’ecografia dell’addome superiore conferma la presenza di epato‑ e splenomegalia, senza che in queste fasi siano in genere evidenti altre alterazioni di rilievo a carico di questi organi.
Diagnosi
Come già accennato in precedenza, in molti pazienti affetti da epatite cronica non è possibile risalire anamnesticamente ad un episodio epatitico acuto o al momento dell’avvenuto contagio: spesso il riscontro di un aumento dei valori sierici delle transaminasi risulta pertanto un reperto occasionale in corso di esami di controllo, magari eseguiti per altre cause o per la presenza di sintomi generali e aspecifici quali astenia, facile affaticabilità, dispepsia e dimagrimento. Per una diagnosi corretta di epatite cronica, e prima di intraprendere ulteriori accertamenti, è necessario che l’ipertransaminasemia sia persistente da almeno sei mesi, o addirittura da un anno. Sarà poi opportuno escludere tutte le potenziali cause di epatopatia su base tossica (farmaci, agenti chimici ecc.) o metabolica (dislípidemia, alterazioni del metabolismo del ferro o del rame ecc.), e naturalmente eseguire un’ampia analisi virologica (vedi oltre) ed immunologica.
Successivamente, soltanto con un esame istologico tramite biopsia epatica sarà possibile stabilire l’effettivo grado di compromissione epatica: già con la colorazione standard all’ematossilina‑eosina è possibile un’analisi soddisfacente, che potrà essere associata a colorazioni specifiche per determinare l’entità della fibrosi o l’eventuale accumulo di ferro. Il quadro istologico tipico dell’epatite cronica è caratterizzato da un infiltrato flogistico costituito da linfociti, monociti, cellule istioidi e plasmacellule, che invade gli spazi portali, interessando più o meno estesamente il parenchima circostante oltre la lamina limitante, che appare interrotta in più punti (peripheral piecemeal necrosis). Glispazi portali appaiono notevolmente ingranditi, con una fibrosi più o meno estesa e neoformazione duttulare. In regione intralobulare, gli epatociti comunemente presentano una necrosi parcellare cui si associano tipici fenomeni regressivi quali palloriamento nucleare, rigonfiamento torbido e frequentemente steatosi; inoltre, le cellule di Kupffer sono aumentate di numero e di dimensioni e sporgono all’interno del lume dei sinusoidi (Fig.03).
Soprattutto nelle fasi di riacutizzazione delle forme da virus B dell’epatite, sono spesso ben evidenti i tipici corpi acidofili, espressione di addensamenti di tipo eosinofilo di derivazione epatocitaria, nonché le caratteristiche cellule a vetro smerigliato (ground glass cells), il cui citoplasma contiene inclusioni eosinofile che spostano il nucleo verso la periferia: queste cellule sono ben evidenti in corso di epatopatia cronica HBsAg positiva, ma sono riscontrabili frequentemente anche in portatori sani (fig.04 fig.05). Con specifiche colorazioni, quali ad esempio l’impregnazione argentica, potranno essere messe in evidenza le alterazioni della trama reticolare, che può apparire frammentata in più punti all’interno del lobulo, mentre è ispessita ed addensata in corrispondenza degli spazi portali (Fig.06).
Con il progredire del processo flogistico, saranno facilmente riconoscibili i setti connettivali, riccamente infiltrati da elementi infiammatori e talvolta capillarizzati (setti attivi). Dagli spazi portali, questi setti si estendono verso il centro del lobulo ed anche tra un lobulo e l’altro, raggiungendo gli spazi portali adiacenti (setti porto‑portali), e le vene centrolobulari (setti porto‑centrali, cui è attribuita una grande importanza nella patogenesi dell’evoluzione cirrogena). Infine, con la comparsa dei noduli di rigenerazione, il quadro istologico assumerà le caratteristiche tipiche di una cirrosi macro‑ o micro‑nodulare.
Secondo la classificazione istopatologica proposta da Knodell et al. (1981), la severità di un’epatite cronica viene determinata con metodo semiquantitativo di graduazione di alcuni parametri fondamentali (Tab.02), il che permette di ottenere un determinato punteggio numerico.
E’ importante a questo punto sottolineare che, se da una parte questo sistema a punteggio costituisce un importante mezzo di ausilio nella pratica clinica, anche per l’indubbio vantaggio di poter valutare agevolmente gli effetti di eventuali terapie, dall’altra non deve sostituirsi in toto alla descrizione per esteso dei quadri esaminati (Tab.03). Gli innegabili vantaggi derivanti dall’utilizzo dell’indice di Knodell sono l’estrema diffusione e quindi l’ampio utilizzo nella pratica clinica e nella valutazione anche comparativa di trials terapeutici, ma soprattutto l’ampio range di punteggio otteníbile, che consente diagnosi estremamente fini. Tuttavia, i primi tre parametri considerati rappresentano una graduazione della malattia, e pertanto sono suscettibili di modificazioni anche in senso regressivo (verso un miglioramento) delle alterazioni osservate, mentre la quantificazione della fibrosi rappresenta un criterio di stadiazione, rappresentando un fenomeno quasi sempre progressivo ed irreversibile. Per questi motivi, molti preferiscono separare questi due aspetti, fornendo i loro referti istologici di punteggi separati.
Nella revisione proposta da Scheuer nel 1991, è stato pertanto suggerito l’impiego di un criterio di stadiazione sulla base dell’entità della fibrosi, secondo quanto descritto nella Tab.04.
Per la caratterizzazione eziologica, è necessario un completo screening virologico, con la ricerca dei marcatori di infezione da HBV in atto (HBsAg, FIBeAg ed HBVDNA nel siero, HBcAg nel tessuto epatico), HCV (anticorpi anti‑HCV con metodica ELISA o con immunoblotting e HCV‑RNA tramite PCR) ed HDV (anticorpi anti‑HDV). In seguito andrà valutata l’eventuale presenza di autoanticorpi circolanti (inizialmente ANA, ASMA, anti‑LKM ed AMA), ed escluse le altre cause di epatopatia cronica (forme causate da farmaci, emocromatosi, morbo di Wilson, deficit di (al‑antitripsina).
Qualora sia già nota un’eziología virale dell’epatopatia, è comunque opportuna la periodica rivalutazione del pattern virologico del paziente, specie in presenza di un improvviso e altrimenti inspiegabile peggioramento clinico e bioumorale. Inoltre, dato che l’HDV può determinare l’inibizione della sintesi e del rilascio in circolo dell’HBsAg, è allora consigliabile eseguire la ricerca dei marcatori FIDV anche in coloro che presentino un’isolata positività degli anticorpi anti‑HBc.
Nelle forme sostenute dall’HCV, che sono quelle di gran lunga più frequenti, un fondamentale indice diagnostico è rappresentato dalla determinazione, quantitativa e qualitativa, dell’HCV‑RNA tramite PCR Il test dovrà essere eseguito in tutti i pazienti anti‑HCV positivi, anche se con transaminasi normali (vedi oltre), al fine di un monitoraggio continuo. Inoltre, la ricerca del genoma virale può rappresentare un utile mezzo diagnostico qualora gli anticorpi specifici anti‑HCV siano assenti, quali ad esempio in pazienti immunodepressí o nei casi di recentissima identificazione. La ricerca dell’HCV‑RNA è invece superflua in presenza di transaminasi elevate e positività anticorpale, che corrisponde quasi costantemente ad uno stato, viremico, nei casi in cui non sia necessario quantificare l’entità della replicazione virale o caratterizzare il genotipo. Nei pazienti anti‑HCV positivi ma con transamínasi normali la determinazione dell’HCV-RNA è invece in ogni caso utile, in quanto un test negativo sarà indice di un’infezione pregressa, mentre un risultato positivo indica un’infezione (ed un’infettività) in corso nonostante la normalità dei test biochimici, e richiede quindi una più attenta vigilanza.
Come già accennato nella parte introduttiva, la diagnosi differenziale si pone nei confronti della cirrosi, nonché delle altre forme di epatopatia cronica (alcolica, da farmaci, da deficit di oci‑anfitripsina, emocromatosi, morbo di Wilson, cirrosi biliare primitiva e colangite sclerosante primaria). L quindi opportuna la valutazione di parametri specifici come il dosaggio dell’ecl‑antitripsina, della ferritina, della ceruloplasmina, della cupremia e della cupruria, ed un’accurata anamnesi, volta a stabilire l’abuso alcolico o l’assunzione di farmaci potenzialmente epatolesivi. In molti casi, peraltro, è solo l’esame bioptico a consentire la diagnosi definitiva, anche perché permette la determinazione quantitativa del contenuto di ferro e di rame intracpatico. t importante sottolineare che spesso la determinazione della reale attività di malattia sulla base di un unico esame istologico può non essere sufficiente, per cui in alcuni casi è necessario un monitoraggio prolungato e integrato da dati clinici e laboratoristici ripetuti nel tempo al fine di stabilire se la malattia tende o meno ad un progressivo aggravamento. Questo approccio metodologico è particolarmente indicato per le forme sostenute dal virus C, dove si può avere una sia pur lenta evoluzione in cirrosi nonostante la benignità del quadro clinico, bioumorale ed anche istologico.
La cirrosi conclamata è in genere clinicamente ben distinguibile dalle altre forme di epatite cronica, qualora siano già evidenti i segni di compromissione parenchimale, con una riduzione dell’attività protidosintetica e catabolica (ipoalbuminemia, riduzione dell’attività protrombinica e del numero delle piastrine, aumento della bilirubina, delle g‑globuline e dell’ammoniemia), associati ad una più marcata epato‑splenomegalía. Inoltre, gli esami strumentali (ecografia ed esofagogastroduodenoscopia) dimostreranno i segni diretti ed indiretti di ipertensione portale (aumento del calibro della vena porta, comparsa di ascite e di varici esofagogastriche). Solo nei casi iniziali, quando cioè la cirrosi non ha ancora determinato i segni di un’ipertensione portale, può essere di ausilio l’esecuzione della biopsia epatica.
Decorso e prognosi
Nonostante l’alternarsi di episodi di riacutizzazione con periodi di relativo benessere, in corso di epatite cronica si osserva raramente la completa e persistente normalizzazione degli esami bioumorali ed in particolare delle transaminasi. Raramente (2‑3% dei casi), la riacutizzazione può essere estremamente intensa, fino a determinare una necrosi epatica massíva o submassiva, con conseguente insufficienza epatica progressiva a esito rapidamente infausto con il quadro tipico della cosiddetta atrofia giafio‑acuta. Secondo la nostra esperienza, nelle forme di epatite cronica da HCV o da HBV la probabilità cumulativa di sviluppare una cirrosi istologicamente evidente è inizialmente abbastanza bassa, e pari a circa il 7% dopo 5 anni dalla diagnosi istologica di epatite cronica, ma tale percentuale tende ad aumentare progressivamente con il prosieguo della malattia, raggiungendo percentuali elevate di incidenza dopo 10 e 15 anni (57% e 87%, rispettivamente), e spesso in assenza di una qualsiasi sintomatologia evidente (Fig.07).
L’importanza di questo dato risiede nel fatto che nella stragrande maggioranza dei casi l’evoluzione di una epatite cronica in cirrosi istologicamente dimostrabile è un fenomeno praticamente costante dopo 15 anni dalla diagnosi istologica, e spesso anche indipendentemente dal trattamento effettuato. Inoltre, tale progressione non appare influenzata dalla diversa eziologia virale della malattia (HCV o HBV) e dal sesso dei pazienti.
Alla comparsa di una cirrosi evidente solo all’esame epato‑bioptico non si accompagnano peraltro i segni di un peggioramento della sintomatologia clinica, che invece si verificano in genere dopo alcuni anni (in media 5‑10), quando cioè si manifesteranno i caratteri clinici dell’ipertensione portale, della ritenzione idrosodica e dell’insufficienza parenchimale.
Nei pazienti affetti da epatite cronica da HBV (che presentano quindi una positività per l’HBsAg, che rappresenta il marcatore più importante ai fini diagnostici), la prognosi è peggiore in presenza dell’HbeAg e dell’HBV‑DNA, laddove la sieroconversione ad anti‑HBe, pur essendo frequentemente anticipata da una riacutizzazione della malattia, si associa ad una evoluzione più lenta e quindi più favorevole; d’altra parte, nei casi in cui la mancanza dell’HBeAg è dovuta all’emergere di una variante “mutata” del virus, incapace cioè di produrre tale antigene, l’evoluzione è più rapida del previsto. Infine, le forme HBV correlate con superinfezione da HDV presentano un decorso più rapido, talvolta fulminante. Solo raramente è osservabile una remissione clinica completa, cui corrisponde istologicamente un quadro di fibrosi epatica: è invece più frequente la stabilizzazione del processo flogistico, associata ad un miglioramento o alla scomparsa della sintomatologia clinica ed alla normalizzazione più o meno completa e duratura delle alterazioni bioumorali; istologicamente si apprezza la riduzione dell’infiltrato flogistico, che rimane confinato nello spazio portale. Seppure queste fasi persistano in genere per lunghi periodi, è comunque possibile la ripresa dell’attività del processo, per cui è comunque necessario il monitoraggio nel tempo anche di questi pazienti.
Terapia
Indipendentemente dall’attività di malattia, è opportuno evitare sforzi fisici intensi ed osservare un relativo riposo soprattutto nelle fasi di riacutizzazione; sarà comunque importante astenersi dall’assumere bevande alcoliche e farmaci potenzialmente epatotossici, mentre la terapia con interferone (vedi oltre) è giustificata solo nei casi in cui le caratteristiche cliniche ed istologiche facciano supporre una tendenza evolutiva della malattia. L’atteggiamento più corretto da seguire è quindi l’attento monitoraggio nel tempo dei parametri clinici e laboratoristici di funzionalità epatica, per stabilire tempestivamente se e quando tali forme mostrano una tendenza alla progressione. In presenza di alterazioni bioumorali persistenti, del reperto di un’attività replicativa virale e di chiari segni istologici di attività di malattia, occorre invece considerare immediatamente una terapia specifica, eziologica, al fine di prevenire o ritardare quanto più possibile l’evoluzione in cirrosi.
Il trattamento di scelta delle forme di epatite virale cronica si basa da tempo sulla somministrazione di interferone. Gli interferoni (IFN) sono polipeptidi prodotti da cellule quali linfociti e fibroblasti, e dotati di numerose proprietà antivirali ed immunomodulanti (quali l’inibizione della traslazione dell’RNA virale e la stimolazione dell’espressione di molecole del complesso VILA da parte delle cellule limitrofe). Gli interferoni attualmente noti sono l’alfa‑2a ed il 2b, prodotti prevalentemente dai linfociti, il beta, prodotto dai fibroblasti, ed il gamma, secreto da numerosi tipi cellulari, ma solo il tipo alfa (ricombinante o linfoblastoide), ed in misura minore il beta, si sono dimostrati efficaci.
E’ essenziale che ogni trattamento, indipendentemente dall’eziologia del processo epatitico cronico, sia proceduto da una stadiazione accurata, sia da un punto di vista ematologico che istologico, al fine di escludere la presenza di patologíe concomitanti e di stabilire l’entità della flogosi, della necrosi e della fibrosi e di accertare l’eventuale presenza di rigenerazione nodulare, che di per sé limita molto la possibilità di una risposta alla terapia con interferone. Nella Tabella 5 sono indicati i parametri clinici identificati come predittívi di risposta positiva e protratta a seguito di un trattamento con interferone alfa.
Periodici controlli sono necessari anche durante il trattamento: le transaminasi non correlano con l’entità dell’epatopatia, ma rappresentano comunque un importante indicatore nel monitoraggio della risposta all’IFN nel tempo, oltre ad essere un test poco costoso ed altamente riproducibile. Ad intervalli meno ravvicinati sarà opportuna anche la determinazione dell’HBV-DNA e dell’HCV-RNA, che rappresentano un indice di replicazione virale e la cui scomparsa nel siero è da considerare pertanto l’obiettivo primario della terapia.
Epatite cronica attiva HBV correlata: iltrattamento di scelta per le forme HBeAg positive prevede la somministrazione di IFN‑(a ricombinante alla dose di 510.000.000 di unità tre volte la settimana, per 4‑6 mesi. Questo tipo di trattamento si è dimostrato in grado di indurre la normalizzazione delle transaminasi (risposta biochimica), di arrestare la replica virale (risposta virologica), con scomparsa dell’HBeAg e dell’HBV-DNA e comparsa degli anticorpi anti‑HBe, nel 50% circa dei casi e di indurre la negativizzazione dell’HBsAg e la sieroconversione ad antiHBs nel 20% (eradicazione completa dell’infezione). In questi casi, la percentuale di recidive durante il follow‑up è di circa il 10%. In studi prospettici, è stato inoltre osservato un significativo aumento della sopravvivenza ed una riduzione dell’incidenza di complicanze dovute alla cirrosi in quei pazienti in cui, ottenuta la sieroconversione ad anti‑Hbe, il trattamento è stato protratto a lungo (fino a 50 mesi).
Nelle forme sostenute da varianti mutate dell’HBV, HBeAg difettive (ovvero anti-HBe ed HBV‑DNA positive), il dosaggio del farmaco deve essere maggiore, pari a 10.000.000 unità tre volte la settimana, per almeno 12 mesi. Con questo schema terapeutico è possibile ottenere la normalizzazione delle transaminasi e soprattutto la negativizzazione dell’HBVDNA in circa il 60‑80% dei casi, ma la percentuale di recidive entro il primo anno dalla sospensione è estremamente elevata, raggiungendo l’80%. Un analogo trattamento viene proposto anche per le forme HDV correlate, ma anche in questo caso i risultati non sono esaltanti e la percentuale di recidive è elevata. Sono attualmente in corso numerosi studi volti a verificare l’efficacia di terapie con interferone associato a farmaci ad attività antivirale quali la timosina, che in uno studio randomizzato si è dimostrata più tollerabile ed altrettanto efficace rispetto all’IFN‑cc, anche in pazienti antiHBe ed HBV‑DNA positivi, e la lamivudina, già da tempo impiegata nella profilassi della reinfezione post‑trapianto, e che si è dimostrata efficace, anche in monoterapia (in certi studi più dell’IFN) in termini di risposta umorale, virologica (negativizzazione dell’HBV-DNA) ed istologica, anche se le recidive sono risultate assai frequenti alla sospensione del trattamento.
Epatite cronica attiva HCV correlata: è ancora poco noto l’esatto meccanismo d’azione dell’IFN nei confronti dell’HCV e degli epatociti da esso infettati, anche se sembra ormai certo che l’attività terapeutica sia basata sull’inibizione dei processi di replicazione virale. Nei numerosissimi trials clinici condotti fino ad oggi è stato dimostrato che terapie basate sulla somministrazione di 3 milioni di unità di IFN‑(x (2a o 2b) tre volte la settimana per 6 mesi consentono di ottenere la normalizzazione delle transaminasi nel 50% circa dei casi, mentre una risposta protratta nel tempo, al termine della cura e durante il followup, si osserva in meno del 20% circa dei pazienti. D’altra parte, è possibile ottenere una negativizzazione dell’HCV-RNA nel 35% circa dei casi al termine del trattamento, e nel 20% nel corso del follow‑up. Le percentuali di risposta positiva e prolungata aumentano fino al 30% qualora il trattamento sia condotto per 12 mesi, come spesso è necessario nelle forme sostenute dal genotipo i dell’HCV, o quando si impieghino dosi maggiori di interferone (5 ‑ 6 milioni di unità tre volte la settimana). Nei casi responsivi alla terapia con IFN, al miglioramento biournorale e alla scomparsa dei marcatori di replicazione virale si accompagna anche un miglioramento sul piano istologico, evidenziato da una riduzione della flogosi e della necrosi epatocitaria. Un nuovo tipo di interferone, ottenuto con tecniche di bioingegneria dall’analisi delle sequenze aminoacidiche degli interferoni naturali e denominato interferone “alfacon‑1”, è stato di recente utilizzato in trial clinici: questa molecola possiede un’ornologia pari all’89% con HFN alfa ed il 30% con il beta, ed in vitro è dotato di un’attività biologica molto più elevata, presumibilmente per una maggiore affinità con i recettori di membrana cellulare. Nel trattamento dell’epatite cronica HCV-correlata, l’IFN alfacon- i (alla dose di 9 pg 3 volte la settimana) si è dimostrato di efficacia e tollerabilità sovrapponibile all’1FN-(x 2b in termini di risposta umorale, e certamente più potente in termini di risposta virologica nei soggetti con genotipo 1 ed alta viremia iniziale. Con la somministrazione di IFN alfacon‑1 a pazienti con recidiva di malattia o con mancata risposta a trattamenti precedenti è stato infine possibile ottenere una sostanziale riduzione della viremia (58% e 13%, rispettivamente); sono in corso di esecuzione alcuni trials clinici condotti su più ampie casistiche al fine di valutare la reale efficaci a di questo nuovo interferone rispetto a quelli attualmente impiegati.
Come già accennato, una stadiazione (sia istologica che bicumorale) della malattia è necessaria in tutti i pazienti prima di intraprendere un trattamento interferonico, anche al fine di ricercare quei parametri che si sono rivelati predittivi di una risposta positiva (Tab.05). Indispensabile è anche un controllo continuo e costante dei parametri bíoumorali durante la terapia, sia per evidenziare eventuali effetti collaterali (vedi oltre), sia perché una mancata risposta biochimica e virologica dopo 3 mesi di trattamento rappresentano un indice prognostico altamente negativo sul risultato finale. La biopsia epatica costituisce una tappa fondamentale prima di intraprendere una terapia con interferone anche dal punto di vista prognostico: infatti, un basso grado di flogosi e la scarsa fibrosi, associati all’assenza ístologica di cirrosi, rappresentano anch’essi un criterio predittivo di risposta positiva.
Per quanto le percentuali di risposta positiva siano abbastanza basse, EFN non è controindicato in presenza di cirrosi ístologicamente evidente: qualora invece l’epatopatia sia evoluta ad uno stadio tale da presentare un’avanzata insufficienza parenchirnale, associata ad ascite ed encefalopatia, allora la terapia interferonica è da evitare del tutto, in quanto potrebbe peggiorare il decorso della malattia.
Numerosi effetti collaterali, più o meno gravi, possono essere osservati durante un trattamento interferonico . Alcuni di essi sono transitori (sintomatologia simil-influenzale caratterizzata da febbre, artralgie e cefalea), e spesso si attenuano nel prosieguo della terapia, essendo inoltre ben controllabili con l’assunzione di paracetamolo. Più raramente (meno del 2% dei casi) si possono osservare disturbi psichici (depressione, talvolta grave, con tendenze suicide) o neurologici (epilessia), patologie autoimmuni (diabete e, tardivamente, tiroiditi), tra cui anche un caso di cirrosi biliare primitiva insorta in corso di terapia per un’epatite cronica HCV‑correlata.
Dall’analisi dei risultati ottenuti in trial clinici condotti associando la ribavirina (5-6 compresse da 200 mg/die per os) all’IFN 2b (3 MU 3 volte la settimana) è emerso che tale associazione consente di ottenere percentuali sensibilmente più elevate, e pari al 46% circa di risposta virologica protratta nel tempo. Questi recenti risultati aprono nuove interessanti prospettive nell’ambito della terapia dell’epatite cronica HCV correlata, specie in quei sottogruppi di pazienti inizialmente non responders ocon infezione sostenuta dai genotipi la e 1b dell’HCV, notoriamente meno sensibili al solo interferone.
La ribavirina sembra essere un farmaco abbastanza maneggevole e con pochi effetti collaterali, rappresentati essenzialmente da un’anemia emolitica reversibile, che comunque richiede di rado una sospensione, ma più spesso una diminuzione del dosaggio. Altri effetti ben noti di questo composto sono quelli teratogeni. L’unico altro inconveniente può essere rappresentato dall’intolleranza gastrica all’alto numero di compresse giornaliere, elemento che può ovviamente richiedere una somministrazione frazionata nell’arco della giornata.
EPATITE CRONICA AUTOIMMUNE
La presenza o la comparsa di autoanticorpi, a basso titolo, è un evento abbastanza frequente in corso di infezione cronica da HCV, e più raramente da HBV (ANA a basso titolo) e HDV (LKM3 nel 15 % dei casi): un tale fenomeno è imputabile alla stimolazione sui linfociti B da parte del virus, HCV in particolare, in virtù delle sue proprietà linfotrope, e talora anche agli effetti della terapia interferonica.
L’epatite cronica autoimmune, o lupoide, rappresenta invece una sindrome clinica del tutto indipendente sul piano nosologico, che viene definita come una “malattia infiammatoria cronica del fegato ad andamento progressivo, caratterizzata istologicamente da un’epatite periportale, con necrosi della lamina limitante, e dalla presenza in circolo di anticorpi organo‑ e non organo‑specifici”.
In genere si può affermare che tutte le forme auto-immuni colpiscono più frequentemente soggetti di età giovanile e di sesso femminile, e le regioni del Nordeuropa, dove la prevalenza è assai maggiore rispetto ai paesi dell’area mediterranea. Tra le principali caratteristiche cliniche sono da ricordare le numerose alterazioni dell’immunità umorale e cellulare, quali un aumento della VES e delle g-globuline (con prevalente quota IgG), la riduzione dei fattori del complemento, la positività del RA‑test, ma soprattutto la presenza di autoanticorpi circolanti, ad alto titolo (almeno superiore ad 1:80), rappresentati principalmente, ma non esclusivamente, da anticorpi anti‑nucleo (ANA), anti‑muscolo liscio (ASMA), rivolti in particolare verso l’actina F, anti-microsomi del fegato e del rene (LKM di tipo 1), anti‑citoplasma (LQ ed anti-antigene epatico solubile (SLA). Nei casi incerti, un altro criterio utilizzato per la diagnosi di epatite cronica autoimmune è anche la favorevole risposta alla terapia corticosteroidea ed immunosoppressiva. L’epatite autoimmune può infine associarsi con altre patologie su base autoimmune, tra le quali le più comuni sono la tiroidite di Hashimoto, l’asma bronchiale, l’artrite reumatoide, la sindrome di Sjógren e l’anemia emolitica autoimmune.
L’eziologia dell’epatite cronica autoimmune resta ancora sconosciuta: la ben documentata associazione con altre patologíe autoimmuni e con gli antigení di istocompatibilità HLA‑A1, B8, DR3 e DR4 indica l’esistenza di una predisposizíone genetica. In certi casi la patogenesi del danno epatico sembra attribuibile ad un’aggressione immunomediata verso gli epatociti, innescata da farmaci (metildopa, nitrofurantoina ecc.) o da ipotetici agenti virali (paramixovirus, citomegalovirus) e non sufficientemente modulata o inibita dai linfociti T suppressor: infatti, in corso di epatite cronica autoímmune può essere evidenziabile un’alterata risposta ai test cutanei di stimolo, una riduzione dei linfociti T totali circolanti, ed una ridotta responsività agli stimoli in vitro da parte dei linfociti CD8+. Ciò può quindi favorire l’instaurarsi di una citotossicità cellulare anticorpo‑dipendente diretta contro antigeni autologhi da parte delle altre popolazioni linfocitarie.
La classificazione dell’epatite autoimmune è stata di recente riformulata al fine di discriminare con esattezza le forme virali (generalmente HCV correlate) con associata una componente immunologica anche spiccata, da quelle autoimmuni propriamente dette. Sulla base del diverso pattern autoanticorpale, l’epatite cronica autoimmune viene distinta in più sottotipi, come riportato nella tabella 7.
L’epatite cronica autoimmune tipo III, caratterizzata dalla presenza isolata di anticorpi anti-SLA, è stata descritta nel 1987, ma la sua autonomia nosologica non è ancora accettata da tutti gli autori. Rara in Italia, anche questa forma colpisce generalmente le donne in età fertile. 11 tipo IV, recentemente proposto ed ancora poco caratterizzato, non presenta marcatori autoanticorpali definiti, ma viene considerato tra le forme autoimmuni per l’assenza di altri fattori eziologici documentabili e soprattutto per la positiva risposta alla terapia steroidea e all’immunosoppressione.
Negli ultimi anni, dalla revisione di numerose casistiche di pazienti un tempo ritenuti affetti da epatite cronica autoimmune, è emerso che molti di coloro che risultavano portatori di anticorpi antiLKM, e/o anti-LC erano di fatto positivi anche per gli anticorpi anti-HCV e per l’HCV-RNA sierico. Analogamente, quasi il 50% di coloro che erano ritenuti affetti da epatite cronica di tipo 1 sulla base della positività per gli autoanticorpi ANA e/o SMA sono poi risultati positivi per l’HCV. Tali dati rendono sul piano clinico estremamente ardua la decisione se sottoporre a terapia steroidea oppure interferonica questo tipo di pazienti. Pertanto, l’International Autoimmune Hepatitis Group ha proposto nel 1993 un sistema che considera cumulativamente numerosi parametri clinici, istologici ed ernatologici per ogni singolo paziente (Tab.08), il che consente con discreta approssimazione di distinguere le forme di epatite cronica virale con associata componente immunologica dalle forme autoimmuni propriamente dette. Tuttavia, esistendo casi di epatite cronica autoimmune certa o altamente probabile, pur in presenza di sicuri marcatori virali, allora, è stata introdotta la definizione di “epatite cronica non classificabile”.
Tipo I. Prevale nel sesso femminile, con insorgenza in età giovanile. Gli autoanticorpi caratteristici sono gli ANA e gli ASMA anti‑actina F, che in certi casi possono essere l’unico marcatore anticorpale della malattia. L’ipergammaglobulinernia è generalmente policlonale e di notevole entità (superiore al 30%), e la risposta alla terapia corticosteroidea è in genere soddisfacente, anche a lungo termine. Nel 30% dei casi insorge acutamente ed è rapidamente evolutiva, con ittero intenso, elevata ipertransammasemia e progressiva insufficienza parenchimale. Negli altri casi il decorso è invece subdolo, con astenia, anoressia, febbricola ed amenorrea. Meno frequenti sono le poliartralgie, le polimialgie e la diarrea. E tipo 1 risulta infine meno frequentemente associato con altre patologie autoimmuni extraepatiche (17% dei casi), ed è 6 volte meno frequente rispetto al tipo Il. Nell’ambito dell’epatite autoimmune di tipo I, un’ulteriore distinzione classificativa è basata sul dato immunogenetico: infatti, nelle forme con aplotipo FILA B8 la malattia insorge più precocemente ma risponde ottimamente alla terapia steroidea, analogamente a quelle con HLA DR4, dove i livelli plasmatici di ANA sono sensibilmente più elevati; d’altra parte, nelle forme con HLA DR3 la prognosi è decisamente peggiore.
Tipo II. Questa forma esordisce in età pediatrica (2 ‑ 10 anni) nel 50% dei casi, molto spesso in modo acuto e rapidamente progressivo verso la cirrosi, e ha una prognosi peggiore. Si associa spesso con patologie extraepatiche quali il diabete di tipo I, alcune tiroiditi, l’anemia emolitica autoimmune e la porpora trombocitopenica idiopatica, la vitiligine e l’alopecia. Inoltre, nel 20% dei pazienti è presente una sindrome poliendocrina autoimmune tipo I. Tipici sono gli autoanticorpi anti-LKMl, a titolo superiore a 1:160, mentre assai meno frequenti sono gli anticorpi anti‑LC. Come già ricordato, è estremamente frequente l’associazione tra epatite cronica HCV correlata e positività per gli anticorpi anti-LKMl: per questo motivo, l’epatite autoimmune di tipo Il viene ulteriormente suddivisa in due sottogruppi, come rappresentato nella tabella 9, dove il tipo Il b può essere considerato come una forma di epatite cronica virale con spiccata componente immunologica.
Da ricordare anche che sono stati descritti casi con caratteristiche intermedie tra l’epatite cronica autoimmune ed epatopatie croniche colestatiche quali la cirrosi biliare primitiva e, meno frequentemente, la colangite sclerosante primaria: alcune di esse rappresentano probabilmente un’epatite autoimmune AMA positiva, altre invece sarebbero cirrosi biliari primitive con atipico pattern anticorpale (e negatività per i tipici anticorpi antimitocondriali diretti contro il complesso mitocondriale della piruvico-deidrogenasi). Anche in questo caso la diagnosi definitiva può essere posta solo sulla base dell’evoluzione istologica (con l’eventuale comparsa di alterazioni a carico dei dotti biliari), Ovvero della risposta terapeutica a steroidi ed immunosoppressori.
In generale, l’epatite autoimmune tipo II è caratterizzata da un esordio clinico che può essere in molti casi del tutto indistinguibile da una forma acuta virale; come già osservato, altre volte l’esordio è più subdolo, con febbricola, subittero, astenia intensa ed amenorrea. Più raramente la malattia è di riscontro occasionale, presentandosi con un’alterazione dei parametri ematologici di funzionalità epatica indagati per altre cause. Infine, in una ridotta percentuale di pazienti, la malattia esordisce già con i segni della cirrosi scompensata. Il decorso è assai variabile, essendo spesso caratterizzato da episodi di recrudescenza alternati a periodi di relativo benessere. Generalmente la prognosi è peggiore nelle forme ad insorgenza acuta e comunque in tutti i casi non trattati (mortalità del 30‑40% a sei mesi dalla diagnosi). Qualora all’esame istologico manchino i segni di rigenerazione nodulare e la terapia venga prontamente instaurata, la prognosi è superiore al 90% a 5 anni, mentre scende al 50% nei casi con cirrosi istologicamente già evidente. La compromissíone delle condizioni generali è in genere più marcata rispetto alle forme ad eziologia virale: sono presenti un’evidente epato-splenomegalia, marcato dimagrimento, artralgie, lesioni cutanee maculo-papulose o eritematose, più frequenti al volto, dove possono assumere l’aspetto a farfalla tipico del LES, e febbricola; nei casi più gravi, compaiono anche versamento pleurico e/o pericardico.
Da un punto di vista istologico, gli spazi portali si presentano infiltrati da elementi mononucleati, tra cui prevalgono le plasmacellule (che molti autori considerano come elemento patognomonico), che oltrepassano la lamina limitante ed invadono il parenchima seguendo i ponti porto/portali e porto/centrali nel frattempo formatisi. Nelle fasi più avanzate, ad un tale quadro si sovrappone la rigenerazione nodulare tipica della cirrosi condamata, verso cui la malattia evolve in genere abbastanza rapidamente.
La terapia dell’epatite cronica autoimmune (di qualunque tipo) è molto efficace se instaurata precocemente, e si basa sull’impiego di corticosteroidi, alla dose iniziale di 20/50 mg nelle forme ad elevata attività e di 10‑20 mg di prednisone al giorno in quelle ad attività lieve o moderata. Dopo 2/4 settimane è spesso possibile ridurre progressivamente il dosaggio, impiegando dosi che siano comunque in grado di controllare la malattia e prevenire le ricadute, in genere 5/10 mg di prednisone al giorno. L’associazione con l’azatioprina (50 mg/die) o con 6-mercaptopurina consente di ridurre il dosaggio di steroidi e l’incidenza di effetti collaterali.
In circa 9 60% dei casi, tale terapia è in grado di indurre e mantenere una remissione istologica, anche se per ottenere la remissione completa dei sintomi e la normalizzazione dei parametri ematochimici è talvolta necessario un trattamento ben più prolungato (oltre i tre anni). In una percentuale elevatissima di casi all’interruzione della terapia si accompagna una rapida ripresa di malattia, mentre per i non responders ab inítio o per coloro che facilmente presentano frequenti episodi di recrudescenza nonostante una terapia steroidea a dosaggi massimali va considerata l’opportunità di eseguire un trapianto di fegato.
Come cura le epatiti la medicina moderna?
1) Interferone Alfa ricombinante: è un prodotto elaborato geneticamente, autorizzato nel 1986 per il trattamento delle leucemie. E’ la copia di una proteina scoperta nel corpo umano.
2) Ribavirina: antivirale
3) Associazione Ribavirina+Interferone Alfa
4) Acido Ursodesossicolico: acido biliare
5) Ipericina: medicinale
6) Timosina: è una proteina prodotta dal corpo umano ed è’ riconducibile alla ghiandola del Timo
7) Inibitori della proteasi:
8) Terapia del Ribozima: enzimi che causano la scissione catalitica di un RNA identificato
9) Amantadina: farmaco usato per il morbo di Parkinson
10) Ofloxacin: antivirale
11) Terapie con Ciclosporine: potente immunosopressore
12) Trapianto
– Effetti collaterali dell’interferone
– Nausea e vomito
– Caduta dei capelli
– Stanchezza: è un sintomo dell’epatite che può amplificarsi con l’uso dell’interferone
– Problemi alla bocca: secchezza
– Infezioni: l’interferone può far diminuire il numero dei globuli bianchi
– Esistono dei rimedi alternativi?
1) Riflessologia
2) Reiki
3) Omeopatia
4) Medicina cinese: tasso dichiarato del 56 % con la maggior parte dei pazienti che mostrano buoni miglioramenti, fu ottenuto con la somministrazione della seguente formula:
Astragula 30g
Salvia 30g
Forsythia 30g
Red peony 30g
Ho-shu-wu 15g
Crateagus 15g
Moutan 15g
Gardenia 15g
Dandeloin 15g
Bupleurum 10g
le erbe vengono decotte e la quantità indicata viene presa e divisa in due dosi che vengono assunte giornalmente per 3 mesi.
5) Ozono terapia: rimozione di una certa quantità di sangue, che viene arricchita con ozono per poi essere reintrodotta nel corpo in modo tale da uccidere i virus.
6) Tarassaco: la radice fa bene per tutti i problemi di fegato, incluse cirrosi, itterizia.
7) Latte di Cardo: esso stimola la rigenerazione delle cellule del fegato e funge da antifiammatorio e stabilizzatore di cellule.
8) Carciofo: una lunga tradizione popolare è stata dimostrata verificando gli effetti rigenerativi e protettivi del carciofo nei confronti del fegato.
9) Radice di liquirizia: studi hanno dimostrato che un componente della liquirizia è efficace nel trattamento dell’epatite virale cronica. Infatti la Glicirrizina ha un’attività antivirale.
10) Spirulina: estratto di alga verde-blu, contiene una sostanza che mostra un’attività antivirale.
11) Aglio: è un antibiotico naturale
12) Vitamina C: si consiglia da 20 a 50 g al giorno in forma pura.
13) Sostanze naturali che aiutano:
– Astragalo: erba cinese che aumenta la reazione degli anticorpi
– Clorofilla: pigmento di una pianta
– Coenzima Q10: antiossidante che aiuta ad incrementare le cellule T-helper
– Echinacea: erba più popolare del Nord america
– Ginko Biloba: potente antiossidante del sistema nervoso
– Melatonina: ormone della ghiandola pineale con forte attività antiossidante
– Cose da evitare in caso di epatiti:
– Alcool:
– Droghe:
– Caffè ed eccitanti:
– Fumo:
– Sale:
– Molluschi crudi:
– Grassi saturi:
– Arachidi e frutta secca: